4月14日,免疫应答与免疫治疗全国重点实验室(以下简称实验室)白丽教授团队在《Cellular & Molecular Immunology》期刊发表的研究论文《MAIT cell plasticity generates CD4+ MAIT cells that promote HCC progression via metabolic crosstalk with tumor cells》,实验室刘连新教授、张会敏副教授为共同通讯作者,实验室傅思成副教授为本文的第一作者。研究围绕黏膜相关恒定T细胞(MAIT)可塑性在肝细胞癌(HCC)进展中的作用与机制展开,明确了CD4+MAIT细胞通过代谢交互促进肝癌发展的完整通路。
肝细胞癌(HCC)是全球癌症相关死亡的最主要病因之一,现有治疗响应率低,核心原因之一是肝脏独特的区域免疫微环境。黏膜相关恒定T细胞(MAIT)在人肝脏中高度富集,最高可占肝脏T细胞的50%,可识别MHC I类相关蛋白1(MR1)呈递的微生物维生素B代谢产物,激活后快速分泌效应分子与多种细胞因子。既往研究证实MAIT细胞与HCC进展密切相关,但其功能存在促瘤/抑瘤的显著争议,学界普遍认为核心原因是MAIT细胞的亚群异质性;同时,MAIT细胞的可塑性能否产生功能特异的致病性亚群、肿瘤细胞与MAIT亚群间的代谢交互调控机制,此前均未阐明。
核心研究结果
Th17极化的CD4⁺ MAIT细胞是人HCC中IL-17A的核心来源
HCC肿瘤组织中约60%的IL-17A⁺ T细胞为CD4⁺ MAIT细胞,其IL-17A分泌水平显著高于其他MAIT亚群、γδ T细胞及传统T细胞;单细胞测序与体外功能实验证实,该细胞高表达Th17特征基因,呈稳定的Th17极化表型,且其Th17功能不依赖高RORγt表达。
CD4⁺ MAIT细胞由CD8⁺ MAIT细胞分化而来,是MAIT细胞可塑性的核心体现
CD8⁺单阳性MAIT细胞可经CD4⁺CD8⁺双阳性过渡态,分化为终末状态的CD4⁺ MAIT细胞,DN MAIT细胞也可向其分化;TCR依赖/非依赖的强激活信号、肝癌微环境均可促进该分化过程,TCR克隆型分析与拟时序轨迹分析验证了其体内分化来源。
CD4⁺ MAIT细胞通过IL-17A-PPARα通路驱动HCC进展
CD4⁺ MAIT来源的IL-17A结合肝癌细胞IL17RA,上调脂质代谢关键转录因子PPARα,进而增强肿瘤细胞的脂质储存与增殖能力;阻断PPARα可完全逆转IL-17A的促瘤效应,TCGA数据证实该通路相关基因高表达与HCC患者不良预后显著相关。
CD4⁺ MAIT细胞丰度与HCC患者不良临床结局显著正相关
HCC肿瘤组织中CD4⁺ MAIT细胞占比显著高于配对癌旁组织,且占比随HCC的BCLC分期升高而增加;其丰度与肿瘤大小、血清肿瘤标志物(AFP/CA19-9/CEA)、肿瘤增殖活性、免疫抑制微环境特征均呈正相关,高丰度患者总生存期显著更差。
体内实验直接证实CD4⁺ MAIT细胞通过IL-17A发挥促瘤作用
向肝癌荷瘤NSG小鼠回输人CD4⁺ MAIT细胞,可显著加速肿瘤生长,同时增强肿瘤细胞的增殖能力、PPARα表达与脂质储存;抗IL-17A中和抗体可完全逆转该促瘤效应,明确IL-17A是CD4⁺ MAIT细胞发挥促瘤作用的核心效应分子。
肝癌细胞与CD4⁺ MAIT细胞形成代谢交互正反馈环路
肝癌细胞经IDO1催化产生的犬尿氨酸(Kyn),可激活CD4⁺ MAIT细胞的AHR通路,直接上调糖酵解相关基因表达,增强细胞糖酵解水平;活跃的糖酵解可解除GAPDH对IL17A mRNA的翻译抑制,通过转录后调控促进IL-17A大量分泌,进一步放大促瘤效应。
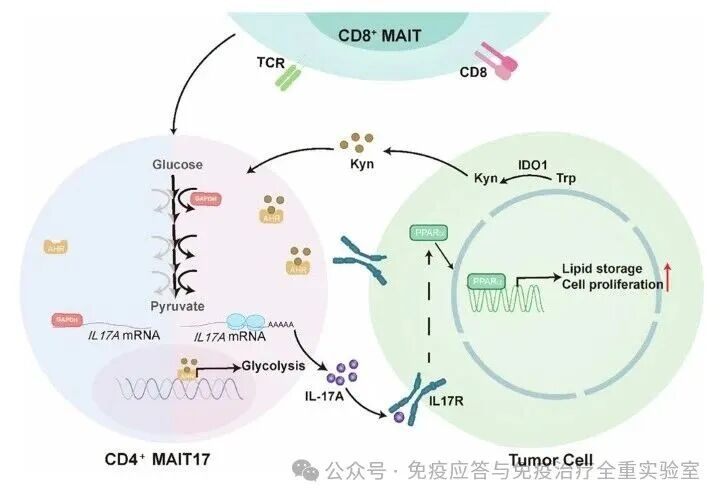
机制图
原文链接:https://www.nature.com/articles/s41423-026-01409-8
