过去很长一段时间里,人们对胃癌的理解主要集中在“异常增殖”这件事上:胃黏膜上皮细胞发生基因改变,逐步摆脱正常生长调控,最终形成恶性肿瘤。这一认识当然没有错,但如果只看到“癌细胞长得快”,其实还远远不够。今天的肿瘤生物学越来越强调,癌症并不是一团孤立扩张的细胞,而是一个不断与宿主发生相互作用的复杂系统。对于胃癌来说,这种相互作用尤其体现在肿瘤细胞与免疫系统、基质细胞、代谢环境乃至微生物因素之间的持续博弈。也正是在这样的背景下,免疫治疗才逐渐从“新概念”变成了胃癌治疗体系中的重要组成部分。
与传统治疗主要直接瞄准肿瘤细胞不同,免疫治疗更像是在重新调整肿瘤与宿主之间的关系。它试图恢复免疫系统对肿瘤的识别和攻击能力,或者至少削弱肿瘤建立起来的免疫抑制状态。对胃癌而言,这一点尤其重要,因为胃癌并不是一种生物学上高度同质的疾病,不同患者的肿瘤在抗原性、免疫细胞浸润水平、炎症状态和免疫逃逸通路上都可能差别很大。换句话说,胃癌不是简单地“能不能用免疫治疗”的问题,而是“哪一类胃癌具有免疫可塑性、能够被重新动员起来”的问题。
一、为什么胃癌值得从免疫角度重新认识
胃癌之所以适合从免疫系统角度重新审视,首先是因为肿瘤的发生和进展,从来不只是癌细胞自身单方面的事情。肿瘤在体内生长时,既要面对宿主免疫监视,也会不断对周围环境施加影响。早期异常细胞有可能被免疫系统清除,但那些最终能够存活、扩增并演化成临床可见肿瘤的细胞,往往已经具备了一定程度的“免疫适应”能力。它们不仅能逃避免疫杀伤,还会主动重塑局部环境,让原本应该参与清除异常细胞的免疫系统逐渐失去效能。
这种认识的意义在于,它把胃癌从一个相对静态的病理实体,转变为一个动态变化的生态系统[2]。癌细胞、T 细胞、巨噬细胞、成纤维细胞、细胞因子和代谢产物共同构成了肿瘤微环境,而免疫治疗的科学基础,正是建立在对这一微环境的重新理解之上。近年的临床指南和综述都强调,胃癌治疗决策越来越依赖分子和免疫特征,例如 PD-L1 状态、MSI/dMMR 状态和 HER2 状态等,这本身就说明:现代胃癌治疗已经不再满足于“看到肿瘤就治疗”,而是更在意这是一种怎样的生物学对象[1]。
二、胃癌是如何逃避免疫系统追杀的
从免疫学角度看,真正危险的不是“有异常细胞出现”,而是这些异常细胞在免疫系统的注视下仍然能够长期存活。胃癌的免疫逃逸并不依赖某一条单一通路,而更像是多层级协同完成的一套“生存策略”。
最常被提及的机制是免疫检查点通路的激活。T 细胞本来是抗肿瘤免疫反应的核心执行者,但它们并不是无限制活跃的,机体为避免过强免疫反应,会设置一些抑制性“刹车系统”。PD-1/PD-L1 就是其中最典型的一条通路。当肿瘤细胞或肿瘤相关免疫细胞表达 PD-L1 时,能够与 T 细胞表面的 PD-1 结合,削弱 T 细胞的增殖能力、细胞毒作用和细胞因子分泌,最终使其进入一种疲惫或低反应状态。免疫检查点抑制剂的出现,本质上就是在试图解除这一抑制。
但胃癌的免疫逃逸显然不止这一层。即使肿瘤内部发生了足够多的基因改变,如果肿瘤抗原处理和呈递环节受损,免疫系统仍可能“看不见”它。换句话说,肿瘤并不一定要强行打退免疫系统,也可以通过降低自身可见度来减少被识别的概率。与此同时,胃癌微环境中常常存在大量免疫抑制性成分,例如调节性 T 细胞、肿瘤相关巨噬细胞以及其他抑制效应 T 细胞活性的因素。这会使局部环境变得越来越不利于有效免疫杀伤。
更进一步看,代谢环境也在参与这场博弈。肿瘤组织常伴随高糖酵解、乳酸堆积、酸化和缺氧,这些改变不仅有利于肿瘤细胞生存,也会影响免疫细胞功能。效应 T 细胞进入这样一个代谢竞争激烈、氧气和营养受限的环境后,往往难以维持理想的活化状态。因此,胃癌免疫逃逸并不是“肿瘤躲起来”这么简单,而是通过检查点抑制、抗原呈递改变、免疫抑制细胞富集和代谢环境重塑等多个层面,逐步把战场改造成更适合肿瘤生存的地方。
三、为什么只有一部分胃癌对免疫治疗更敏感
胃癌免疫治疗最吸引人的地方,恰恰也是它最复杂的地方:并不是所有患者都会从中同等获益。造成这种差异的根本原因,在于不同胃癌的免疫原性和微环境状态并不一致。
其中最具代表性的标志物之一是 MSI-H/dMMR,也就是微卫星高度不稳定或错配修复缺陷。此类肿瘤由于 DNA 修复机制受损,更容易累积大量突变,从而产生更多潜在的新抗原。这意味着肿瘤更可能被免疫系统识别,也更有机会对免疫检查点抑制剂产生反应。正因如此,MSI-H/dMMR 被认为是免疫治疗获益最有说服力的分子依据之一,FDA 也早已基于这一生物学特征给予 pembrolizumab 组织学无关的适应证支持[4]。
另一个常被讨论的指标是 PD-L1 表达。一般来说,PD-L1 表达较高提示肿瘤局部可能存在更活跃的免疫抑制通路,因此统计学上更有可能从 PD-1/PD-L1 抑制中受益。不过,PD-L1 并不是一个绝对指标。它会受到检测平台、评分方法、取材部位和时间变化的影响,而且高表达并不意味着一定有效,低表达也不代表绝对无效。因此,从生物学上理解,PD-L1 更像是一个反映肿瘤—免疫相互作用状态的窗口,而不是一个简单的二元开关。
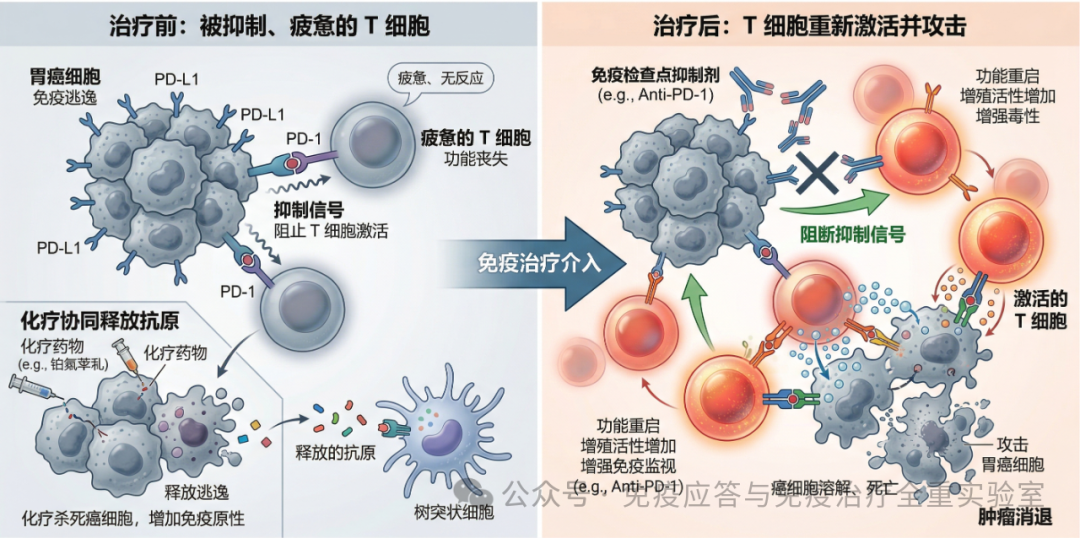
图1:免疫治疗重塑胃癌免疫微环境
除了 MSI-H/dMMR 和 PD-L1,胃癌的免疫敏感性还与更广泛的分子背景有关。例如一些 EBV 相关胃癌往往具有更明显的免疫细胞浸润和更高的免疫活性特征[3]。虽然在日常临床路径中,EBV 并不像 HER2 或 MSI 那样直接决定标准方案,但它提示我们一个很重要的事实:胃癌免疫治疗反应的本质,仍然取决于肿瘤是否具有足够抗原性,是否已有一定免疫识别基础,以及这种识别是否只是被抑制而非彻底缺失。
四、免疫治疗如何改变胃癌的干预逻辑
免疫治疗给胃癌治疗带来的变化,不只是“多了一种药”,而是改变了干预逻辑。过去的治疗思路更偏向于直接压制肿瘤生长,例如手术切除、化疗杀伤和局部治疗;而现在,越来越多的策略开始尝试同时改变肿瘤微环境,让免疫系统重新参与进来。
在这一过程中,免疫检查点抑制剂之所以常与化疗联用,并不是偶然。某些化疗药物除了直接杀伤肿瘤细胞外,还可能促进肿瘤抗原释放,增强抗原提呈,甚至在一定程度上减少部分免疫抑制性细胞,从而为免疫治疗创造更合适的条件。也就是说,化疗和免疫治疗并不一定是“一个负责杀细胞,一个负责调免疫”的简单并列关系,二者在部分情境下可以形成机制上的协同。
近年的关键研究已经把这种协同推进到临床实践中。FDA 在 2023 年批准 pembrolizumab 联合含氟嘧啶和铂类化疗,用于 PD-L1 CPS≥1 的 HER2 阴性局部晚期不可切除或转移性胃癌/胃食管结合部腺癌一线治疗[5]。2025 年又批准 pembrolizumab 联合 trastuzumab 和化疗,用于 PD-L1 CPS≥1 的 HER2 阳性局部晚期不可切除或转移性胃癌/胃食管结合部腺癌一线治疗[6]。这样的进展说明,免疫治疗已经不再是边缘性尝试,而是被纳入特定分层人群的一线治疗框架中。
这些临床研究从更深一层也支持了一个生物学判断:至少在部分胃癌中,肿瘤微环境并非完全“僵死”,而是仍然具有一定的可塑性。外源干预并不能让所有胃癌都变成免疫敏感型,但它确实能够在合适人群中打破部分免疫抑制平衡,争取更持久的疾病控制。
五、从免疫治疗出发,我们重新理解胃癌
如果说免疫治疗对胃癌研究最大的贡献是什么,那也许不是某一种药物本身,而是它迫使我们重新思考胃癌到底是什么。它不再只是显微镜下的一种组织学类型,也不只是影像学上的占位病变,而是一个会在免疫压力下持续演化的动态系统。肿瘤细胞一边适应宿主环境,一边塑造新的微环境,而免疫系统并非始终缺席,只是常常被误导、被削弱,或者被局部压制。
也正因如此,未来胃癌免疫治疗的发展,恐怕不会停留在单纯比较“哪一种 PD-1 抑制剂更好”这一层面。更值得关注的方向,是如何建立更精细的生物标志物体系,如何用空间转录组、免疫浸润谱和分子分型更准确地识别获益人群,以及如何理解原发耐药和继发耐药背后的生物学基础。对生命科学研究者而言,胃癌免疫治疗真正迷人的地方,不仅在于它提供了新的治疗手段,更在于它揭示了一个问题:肿瘤并不是在免疫系统“没看见”的情况下生长起来的,而是在长期博弈中,逐步学会了如何活下来。
从这个意义上说,“胃癌免疫治疗”并不只是一个临床热点名词,它更像是现代肿瘤生物学的一面镜子。透过这面镜子,我们看到的不是一种单纯的新药,而是肿瘤、免疫与微环境之间一场仍在继续的复杂对抗。
何新阳课题组供稿
注:本文为面向生物学方向的科普整理稿,强调机制理解,不替代具体临床决策。Gemini大模型协助图片生成
参考文献:
1.NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Gastric Cancer, Version 2.2026.
2.Schreiber RD, Old LJ, Smyth MJ. Cancer immunoediting: integrating immunity’s roles in cancer suppression and promotion. Annual Review of Immunology. 2011.
3. The Cancer Genome Atlas Research Network. Comprehensive molecular characterization of gastric adenocarcinoma. Nature. 2014.
4.U.S. Food and Drug Administration. FDA grants accelerated approval to pembrolizumab for first tissue/site agnostic indication. 2017.
5. U.S. FDA. FDA approves pembrolizumab with chemotherapy for HER2-negative gastric or gastroesophageal junction adenocarcinoma. 2023.
6.U.S. FDA. FDA approves pembrolizumab for HER2 positive gastric or gastroesophageal junction adenocarcinoma expressing PD-L1 (CPS ≥1). 2025.
