本期目录
1. 揭示NK细胞全新免疫检查点SAMSN1调控HCC发生机制
2. 系统鉴定NK细胞免疫检查点CLEC12B
3. 开发高效广谱抗埃博拉病毒纳米抗体
4. 揭示肝脏清除递送系统的底层机制
5. 揭示性别特异性抗肿瘤免疫中的调控机制
6. 揭示调控CD8⁺ T细胞耗竭进程的关键分子
1、揭示NK细胞全新免疫检查点SAMSN1调控HCC发生机制
2026年2月21日,实验室孙成教授团队在《Nature Communications》发表论文“SAMSN1 restrains NK cell mediated anti-tumor immunity in hepatocellular carcinoma”。该研究首次证实SAMSN1蛋白作为NK细胞免疫检查点分子,其主要功能是抑制HCC中NK细胞的抗肿瘤免疫活性。作者通过整合分析临床患者样本数据与临床前动物模型,系统地揭示了SAMSN1在HCC进展中的关键作用及其作用机制。
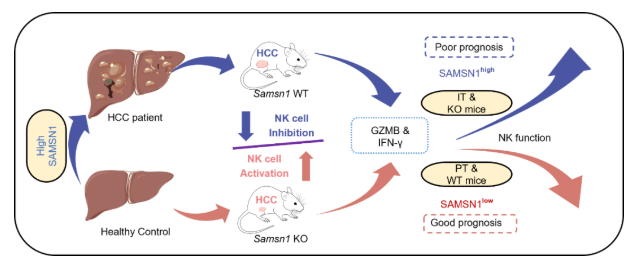
图:野生型小鼠相比Samsn1基因敲除小鼠在Hepa1-6肝原位模型中的肿瘤生长明显抑制同时小鼠生存期显著延长
新闻链接:
https://immune.ustc.edu.cn/2026/0301/c38573a721717/page.htm
论文链接:
https://www.nature.com/articles/s41467-026-68661-4
2、系统鉴定NK细胞免疫检查点CLEC12B
2026年3月17日,实验室孙成教授团队在免疫学顶级期刊《Nature Immunology》上发表题为“Targeting NK cell CLEC12B enhances cancer immunotherapy”的研究论文,系统鉴定了CLEC12B这一NK细胞免疫检查点,深入解析了其调控肿瘤免疫逃逸的分子机制,并率先开发了具有临床转化潜力的靶向纳米抗体,为NK细胞免疫治疗领域提供了具有价值的新靶点与新策略。
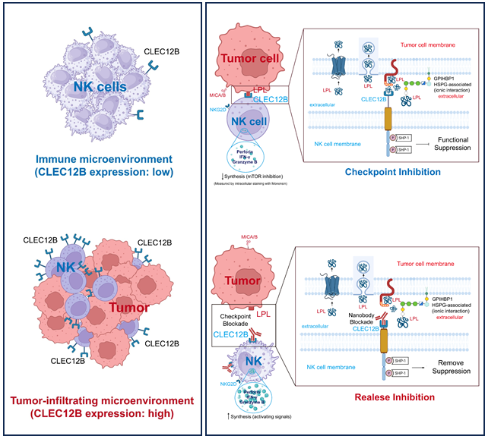
图:在稳态条件下,NK 细胞表现为CLEC12B低表达并保持有效的细胞毒性活性(左图);肿瘤相关的 LPL 结合CLEC12B介导检查点抑制作用。通过 HSPGs 锚定在肿瘤细胞表面的LPL(胞外)与NK细胞上的CLEC12B结合,触发 SHP-1 介导的mTOR抑制并减少效应分子的合成(右上)。H6 纳米抗体阻断CLEC12B-LPL的结合(检查点阻断)。NK细胞的全活化需要双信号:检查点阻断加上激活受体的结合(例如 MICA/B→NKG2D,右下)。
新闻链接:
https://immune.ustc.edu.cn/2026/0321/c38573a723826/page.htm
文链接:
https://www.nature.com/articles/s41590-026-02471-0
3、开发高效广谱抗埃博拉病毒纳米抗体
2026年3月17日,实验室金腾川教授团队在《Nature Communications》期刊在线发表题为“A highly potent nanobody-based bispecific therapeutic provides broad-spectrum protection against ebolavirus”的研究论文。研究团队成功筛选获得两株广谱高效的中和纳米抗体,并基于结构基础设计出双特异性抗体BA2-1A10-Fc,在啮齿动物模型中对多种埃博拉病毒亚型展现出强效保护作用,为广谱埃博拉病毒治疗药物开发提供了全新思路。
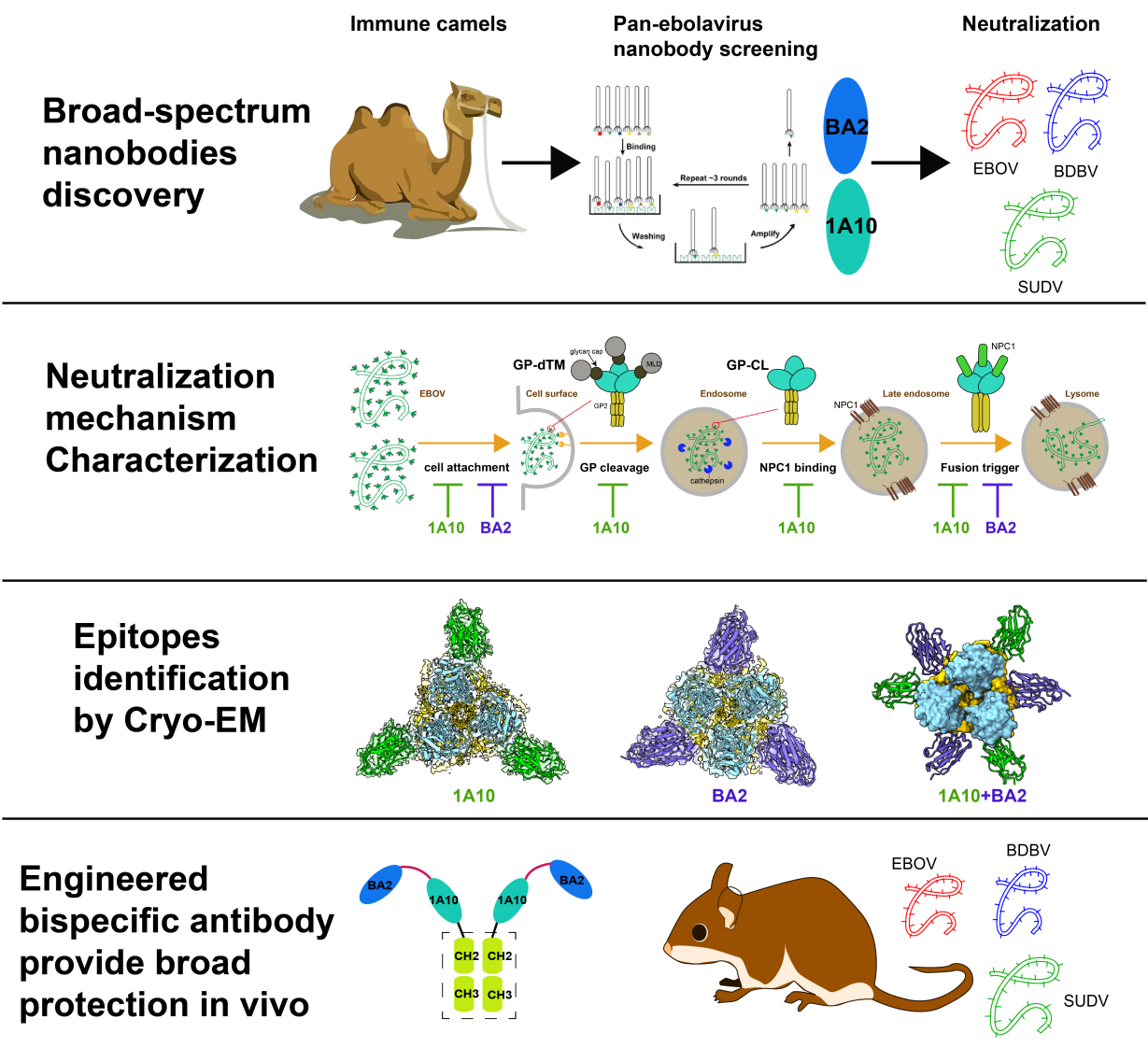
图:文章主要内容摘要
新闻链接:
http://tjlab.ustc.edu.cn
论文链接:
https://www.nature.com/articles/s41467-026-70464-6
4、揭示肝脏清除递送系统的底层机制
2026年3月20日,实验室王育才教授、朱书教授团队在国际权威学术期刊《Science》在线发表了题为 “Commensal-driven serotonin production modulates in vivo delivery of synthetic and viral vectors”的研究论文,首次阐明肠道共生菌与肠道内分泌系统共同维持的肠—肝免疫调控轴,揭示了机体非特异性清除药物递送载体的底层机制。该研究为破解困扰递送领域数十年的核心难题提供了普适性解决方案,显著提升肿瘤靶向治疗、mRNA疗法、基因编辑等疗法的递送效率与治疗效果,为生物医药递送技术的临床转化开辟新路径。
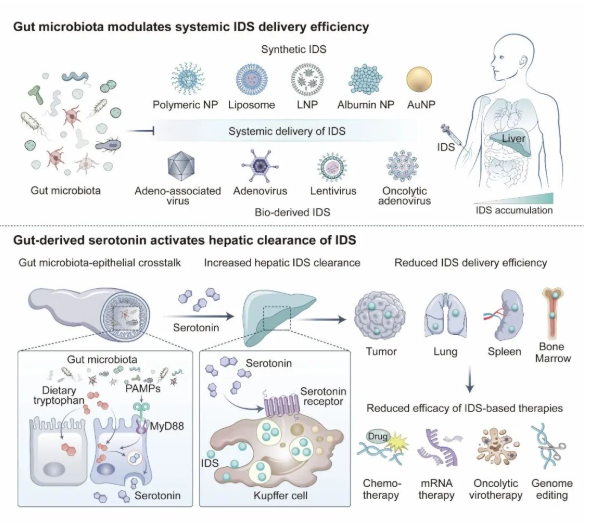
图:肠道共生菌通过刺激肠道五羟色胺分泌维持肝脏对递送载体的清除活性
新闻链接:
https://immune.ustc.edu.cn/2026/0320/c38573a723705/page.htm
论文链接:
https://www.science.org/doi/10.1126/science.adu7686
5、揭示性别特异性抗肿瘤免疫中的调控机制
2026年3月20日,实验室崔国梁教授团队在国际权威学术期刊《Nature Metabolism》上发表题为“DGAT1 mediates sex-specific CD8+ T cell antitumour responses”的研究论文。围绕DGAT1介导的脂质代谢,探索其在性别特异性抗肿瘤免疫中的调控机制,既是填补领域空白,也能为肿瘤免疫治疗的性别分层和代谢靶向联合治疗提供新依据。
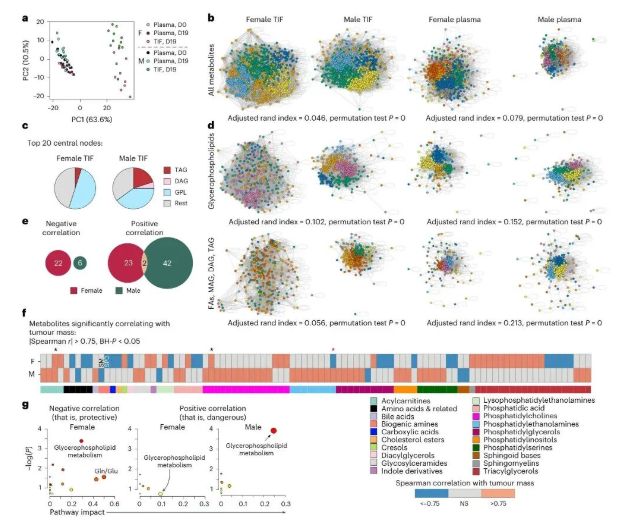
图:雌雄小鼠肿瘤微环境(TME)的代谢差异
新闻链接:
https://immune.ustc.edu.cn/2026/0327/c38573a724307/page.htm
论文链接:
https://www.nature.com/articles/s42255-026-01462-7
6、揭示调控CD8⁺ T细胞耗竭进程的关键分子
2026年3月27日,实验室李丰银教授团队在Journal of Experimental Medicine(JEM) 杂志发表了题为Targeting Mettl8-Tcf1 axis promotes CD8+Tpex differentiation and antitumor immunity的研究论文。该研究首次揭示了RNA甲基转移酶 Mettl8 是调控CD8⁺ T细胞耗竭进程的关键分子,阐明了Mettl8通过稳定Tcf7mRNA和协同Tcf1蛋白维持Tpex细胞干性的双重机制,还发现小分子抑制剂银杏酸(Ginkgolic acid,GA)能与抗PD-1产生协同抗肿瘤效应,为优化肿瘤免疫治疗提供了新思路。
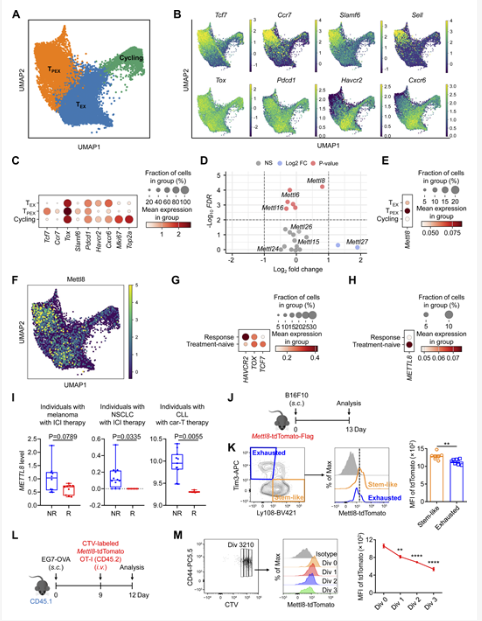
图:Mettl8 在 T PEX 细胞中高表达,在抗 PD-1 治疗后表达降低
新闻链接:
https://immune.ustc.edu.cn/2026/0330/c38573a724567/page.htm
论文链接:
https://doi.org/10.1084/jem.20250424
