本期目录
1. 揭示双位点修饰激活肠道NLRP6炎症小体新机制
2. 揭示EBV感染导致多发性硬化症发生的新机制
3. 揭示调控肺泡巨噬细胞稳态和功能的新机制
4. 阐明妊娠期呼吸道感染致不良妊娠结局的免疫机制并提出DPP4抑制剂双器官靶向治疗新思路
5. 揭示肠道上皮修复的“神经检查点”机制
1、揭示双位点修饰激活肠道NLRP6炎症小体新机制
2026年1月6日,实验室朱书教授团队在Cell Host & Microbe期刊上在线发表题为 “UBE2O-mediated monoubiquitination licenses NLRP6 inflammasome activation in the intestine” 的研究论文。该研究系统揭示了肠道上皮细胞中NLRP6炎症小体活化的新机制——UBE2O介导的双位点单泛素化修饰,通过构象转变依赖的寡聚和空间位阻引发的胞质阻隔这两种位点特异性分子事件协同确保NLRP6炎症小体在细胞质中的激活,为理解肠道黏膜免疫调控提供了新的视角和见解。
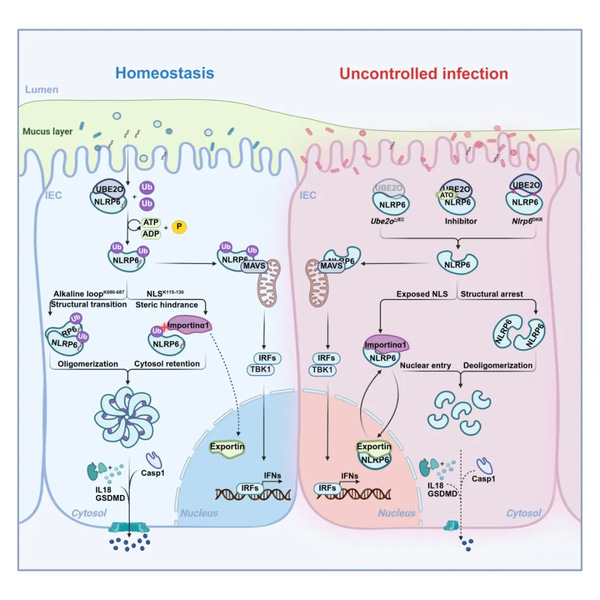
图:双保险激活模型:位点特异的单泛素化通过构象转变和空间转换的协同机制促进NLRP6炎症小体组装
新闻链接:
https://immune.ustc.edu.cn/2026/0108/c40520a719098/page.htm
论文链接:
https://pubmed.ncbi.nlm.nih.gov/41500221/
2、揭示EBV感染导致多发性硬化症发生的新机制
2026年1月14日,实验室王剑教授课题组与苏黎世大学Roland Martin教授课题组合作在《Cell》期刊在线发表题为“EBV Infection and HLA-DR15 Jointly Drive Multiple Sclerosis by Myelin Peptide Presentation”的研究论文。该研究通过免疫多肽谱分析和自身反应性CD4+ T细胞功能鉴定,揭示了爱泼斯坦-巴尔病毒(EBV)感染与人类白细胞抗原HLA-DR15协同作用,通过呈递髓鞘自身抗原多肽并激活自身反应性CD4+ T细胞,共同驱动多发性硬化症(MS)发生的新机制。
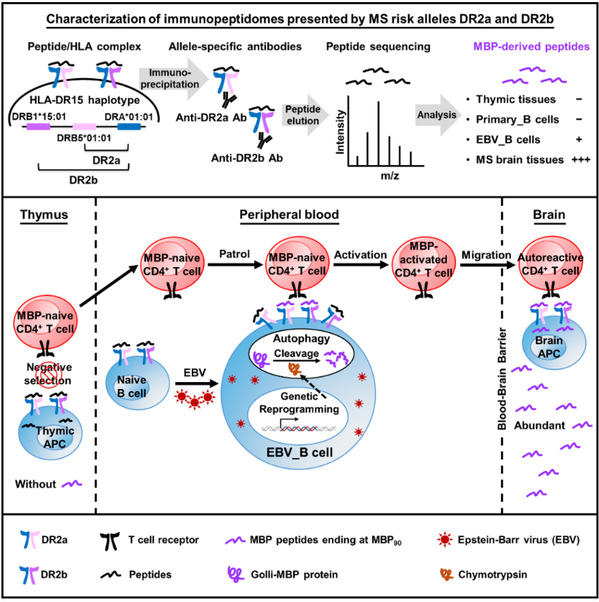
图:激活自身反应性CD4+ T细胞
新闻链接:
https://immune.ustc.edu.cn/2026/0114/c38573a719539/page.htm
论文链接:
https://doi.org/10.1016/j.cell.2025.12.046
3、揭示调控肺泡巨噬细胞稳态和功能的新机制
2026年1月31日,实验室白丽教授课题组在Nature Communications在线发表题为“Microbiota-induced EI24 improves homeostasis but impedes function of alveolar macrophages via metabolic regulation”的研究论文。该研究揭示,共生微生物诱导的EI24在维持AMs稳态的同时,抑制其吞噬功能和炎症因子表达,妨碍了AMs介导的抗肿瘤和抗感染免疫应答。同时,研究还发现EI24广泛抑制多种巨噬细胞功能,为靶向EI24发展巨噬细胞的免疫治疗策略提供了理论依据。
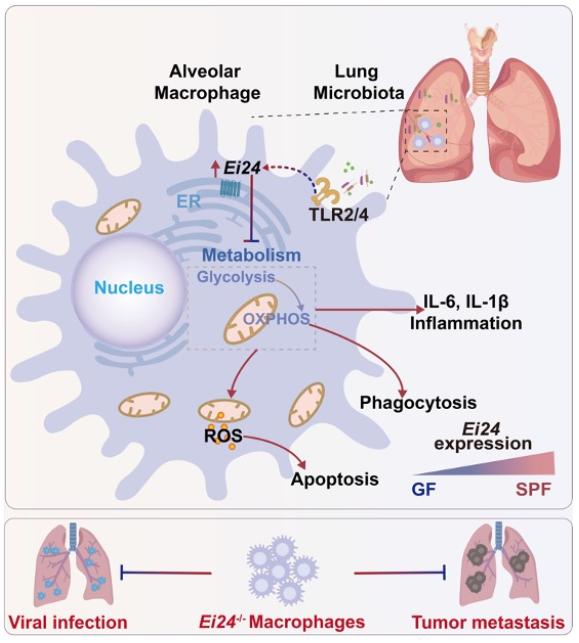
图:给小鼠转输EI24缺失的骨髓来源巨噬细胞,可有效抑制肺脏肿瘤转移和病毒感染,
提示靶向敲除EI24可增强巨噬细胞的免疫治疗疗效。
新闻链接:
https://immune.ustc.edu.cn/2026/0205/c38573a721268/page.htm
论文链接:
https://www.nature.com/articles/s41467-026-69000-3
4、阐明妊娠期呼吸道感染致不良妊娠结局的免疫机制,提出DPP4抑制剂双器官靶向治疗新思路
2026年2月17日,实验室傅斌清教授、魏海明教授团队在Nature Communications杂志,在线发表题为“Dipeptidylpeptidase 4 inhibition attenuates gestational pathologies via immune homeostasis restoration in the pulmonary-uterine axis”的研究论文。该研究揭示,呼吸道病毒感染通过“肺-子宫轴”免疫交叉对话破坏母胎界面稳态的新机制,并创新性地提出DPP4抑制剂可作为一种“双器官靶向”治疗策略,为防治病毒性妊娠并发症提供了重要理论依据和干预新靶点。
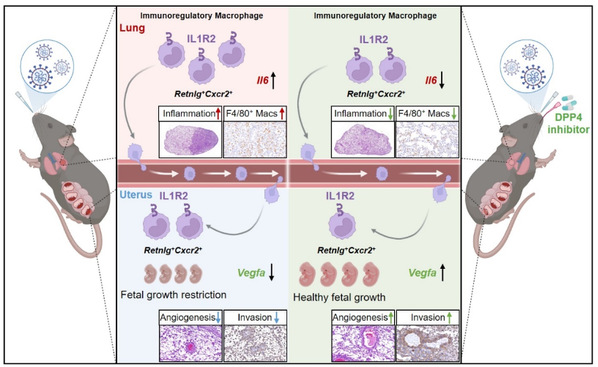
图:妊娠期呼吸道病毒感染通过“肺-子宫轴”免疫交叉对话破坏母胎界面稳态,
而DPP4抑制剂可作为一种“双器官靶向”治疗策略挽救呼吸道病毒感染导致的胚胎生长受限。
新闻链接:
https://immune.ustc.edu.cn/2026/0223/c38573a721574/page.htm
论文链接:
https://www.nature.com/articles/s41467-026-69620-9
5、揭示肠道上皮修复的“神经检查点”机制
2026年2月23日,实验室潘文教授团队在Cell Stem Cell发表论文“VIPR1 acts as an enteric neural checkpoint that suppresses intestinal stem cell-driven epithelial regeneration and exacerbates colitis”,首次提出调控肠道上皮修复再生的“神经检查点”机制。研究揭示,在炎症性肠病 (IBD) 等慢性炎症中,VIP能神经元通过直接激活干细胞受体VIPR1,抑制上皮再生程序,延缓黏膜愈合并加重炎症进展,确立了神经系统对肠道上皮修复的关键门控作用。
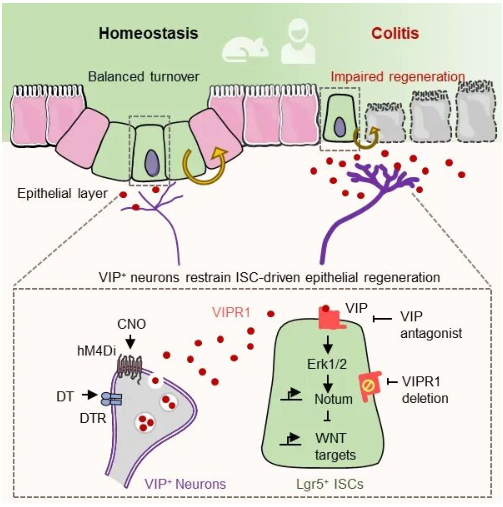
图:VIP信号通过VIPR1-ERK-Notum轴调控干细胞WNT通路
新闻链接:
https://immune.ustc.edu.cn/2026/0225/c38573a721613/page.htm
论文链接:
https://www.cell.com/cell-stem-cell/abstract/S1934-5909(26)00032-9
