免疫应答与免疫治疗全国重点实验室崔国梁教授、安徽医科大学吴晶霞教授、南京医科大学王曦教授和蒂宾根大学Alaa Madi教授等人围绕DGAT1介导的脂质代谢,探索其在性别特异性抗肿瘤免疫中的调控机制,既是填补领域空白,也能为肿瘤免疫治疗的性别分层和代谢靶向联合治疗提供新依据。相关内容以“DGAT1 mediates sex-specific CD8+ T cell antitumour responses”为题发表在《Nature Metabolism》上。

【主要内容】
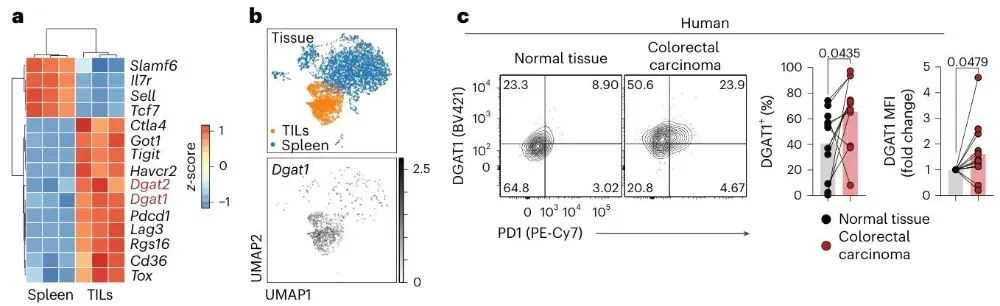
通过批量RNA测序、单细胞RNA测序和流式细胞术分析,发现小鼠B16.F10黑色素瘤模型中,CD8+肿瘤浸润淋巴细胞(TILs)的Dgat1转录水平被选择性上调,表达谱与PD1、TIM3等已知耗竭标志物匹配,而Dgat2表达极低,DIESL及其负调控因子Tmx1则下调,同时在人类结直肠癌患者的CD8+ TILs中,DGAT1蛋白水平也显著高于邻近正常黏膜的CD8+ T细胞,表明DGAT1是CD8+ TILs中主要的三酰甘油合成酶,且其表达与T细胞耗竭相关。
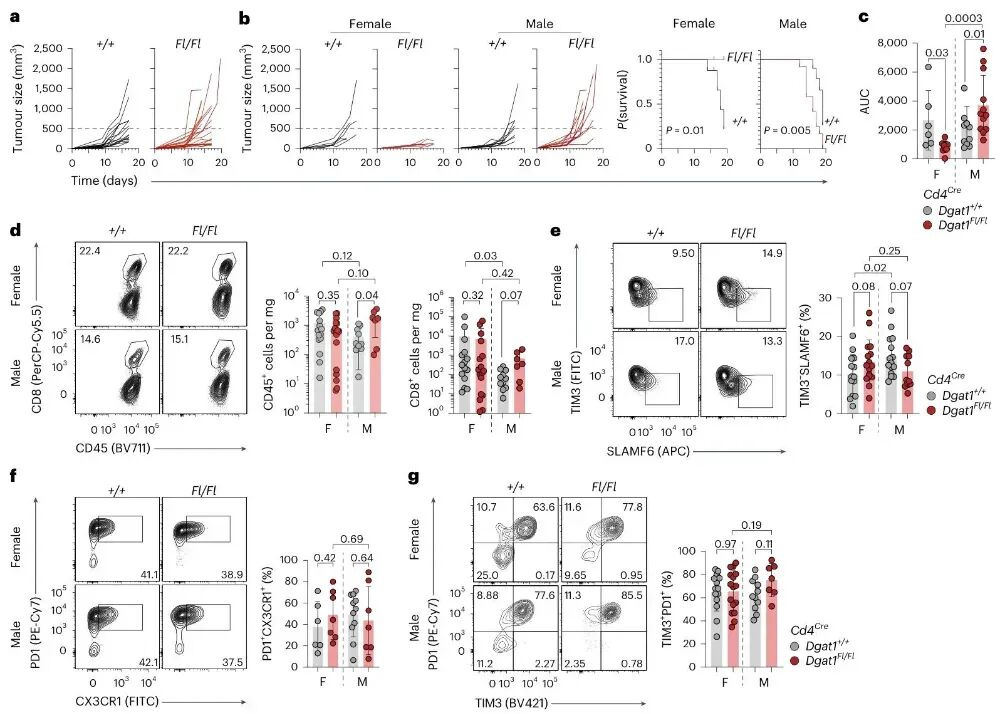
通过在T细胞特异性Dgat1敲除(Dgat1 KO)小鼠和野生型(WT) 同胎仔畜中植入B16黑色素瘤细胞,揭示了DGAT1在肿瘤浸润T细胞中功能的性别二态性,整体数据未显示明显差异,但按性别分层后,雌性Dgat1 KO小鼠能更好地控制肿瘤生长,而雄性Dgat1 KO小鼠肿瘤生长更快,流式细胞术分析显示,肿瘤较小的雌性Dgat1 KO小鼠和雄性WT小鼠中祖细胞样耗竭T细胞(Tₑₓ)有增多趋势,雄性Dgat1 KO小鼠中调节性T细胞(Treg)富集,且这一性别特异性表型在MC38结直肠癌模型中也得到了验证。
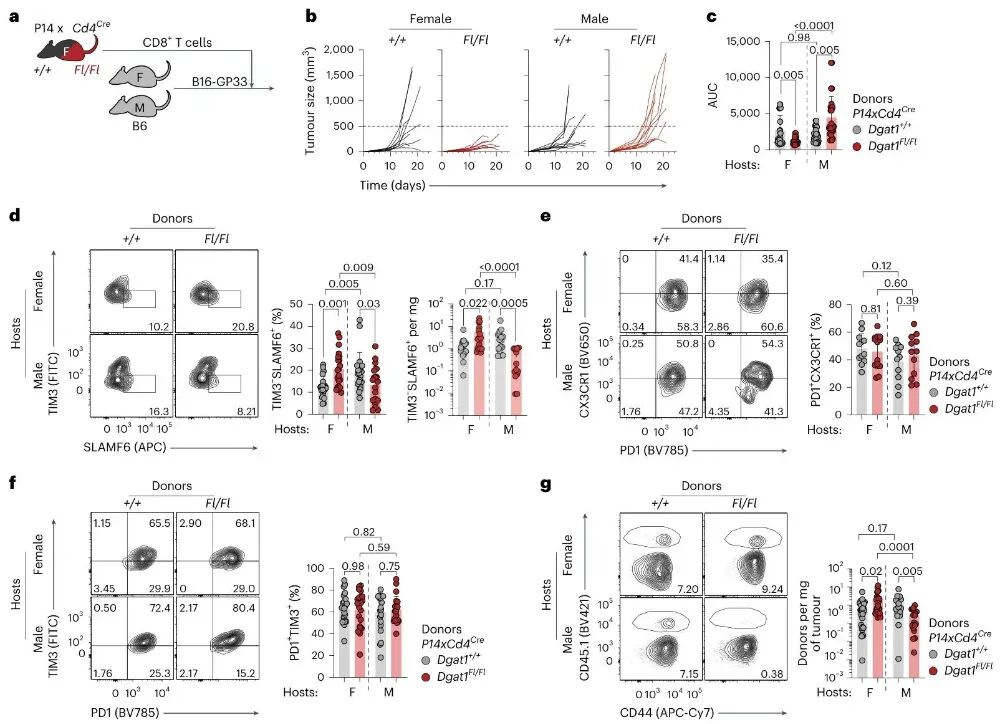
将雌性WT或Dgat1 KO P14细胞转移到荷瘤雌性或雄性宿主后,雌性宿主接受Dgat1 KO P14细胞能更好控制肿瘤,而雄性宿主中Dgat1 KO P14细胞无法抑制肿瘤发展,同时雌性宿主中Dgat1 KO P14细胞的祖细胞样Tₑₓ细胞富集,雄性宿主中该细胞群耗竭,且Dgat1 KO供体TILs在雌性宿主中更丰富,在雄性宿主中更少,而脾脏中供体细胞数量无DGAT1介导的性别差异,表明DGAT1在雄性肿瘤微环境中对维持祖细胞样Tₑₓ细胞和抗原特异性CD8+ TIL群体至关重要。
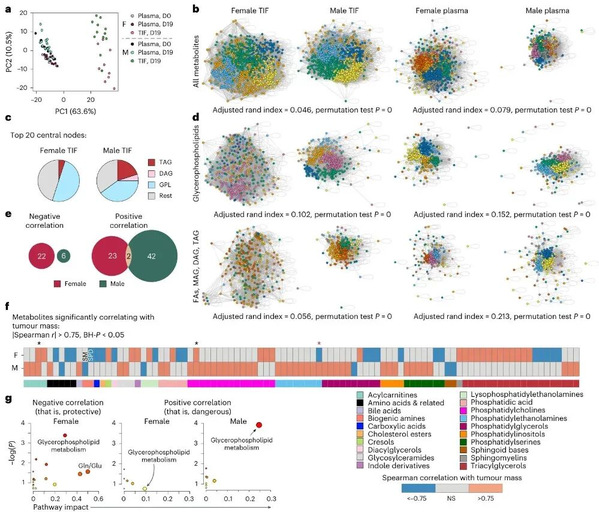
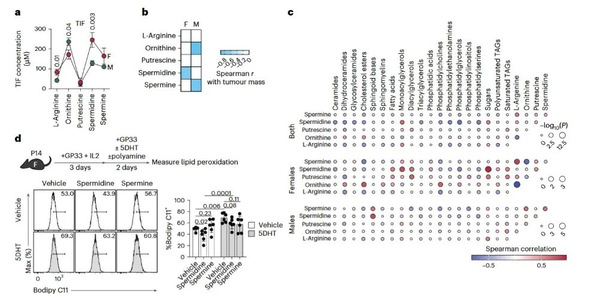
通过对血浆和肿瘤间质液(TIF)的靶向代谢组学分析,主成分分析显示样本按血浆/ TIF和性别显著分离,雄性TIF中三酰甘油(TAGs)和甘油磷脂(如磷脂酰乙醇胺、磷脂酰胆碱)富集,代谢通量和网络分析表明雄性TIF中TAG合成途径整合更紧密,且雄性TIF中含多不饱和脂肪酸链的TAG水平更高,但多不饱和脂肪酸-TAG与饱和脂肪酸-TAG的比值低于雌性,溶血磷脂酰乙醇胺/磷脂酰乙醇胺比值更低,同时与肿瘤质量相关的代谢物和代谢途径也存在性别差异,甘油磷脂浓度在雌性中与较小肿瘤相关,在雄性中与较大肿瘤相关。
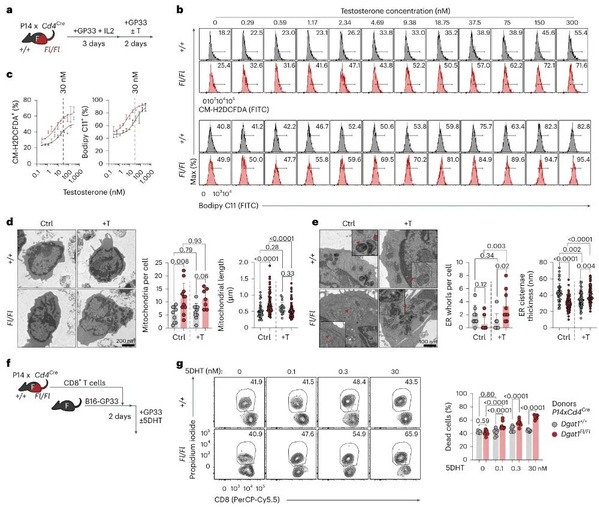
将WT和Dgat1 KO P14细胞经GP33和IL-2激活后,再用不同浓度睾酮处理,发现睾酮会诱导ROS和脂质过氧化物积累,且Dgat1 KO细胞对睾酮更敏感,透射电镜显示,睾酮处理导致Dgat1 KO细胞线粒体数量减少、长度缩短,内质网肿胀并出现洋葱样结构(ER应激标志),同时在5DHT处理的小鼠CD8+ TILs中,Dgat1 KO细胞的死亡率显著升高,表明AR信号与Dgat1缺失结合会诱导氧化应激、ER应激和细胞死亡。
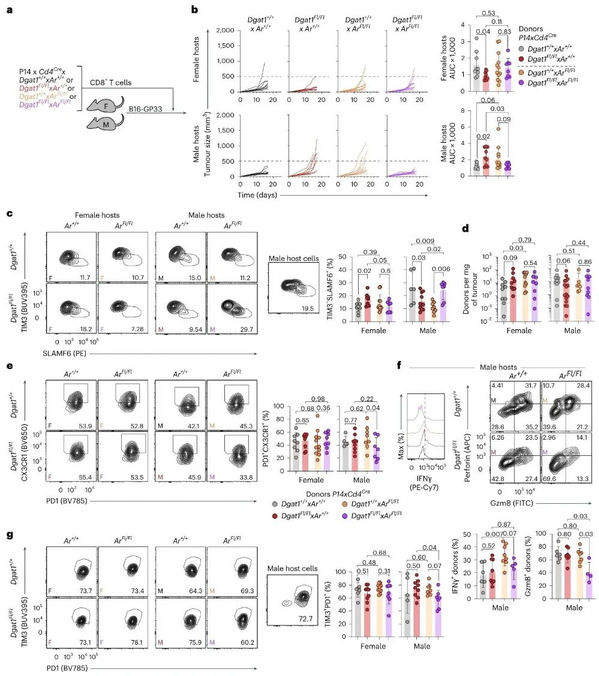
过继转移实验显示,雄性宿主接受Dgat1 × Ar双敲除细胞后,肿瘤大小与接受WT细胞的小鼠相当,挽救了Dgat1单敲除导致的肿瘤生长加速表型,同时双敲除恢复了雄性宿主中祖细胞样Tₑₓ细胞的丰度,减少了下游过渡态和终末耗竭细胞的分化,且Ar敲除会增加IFNγ阳性细胞比例,但该有益效应在Dgat1同时敲除时被逆转,证实AR以CD8+ T细胞内在方式限制Dgat1 KO细胞在雄性中的存活,且其与DGAT1的相互作用依赖微环境中的雄激素浓度和脂质组成。
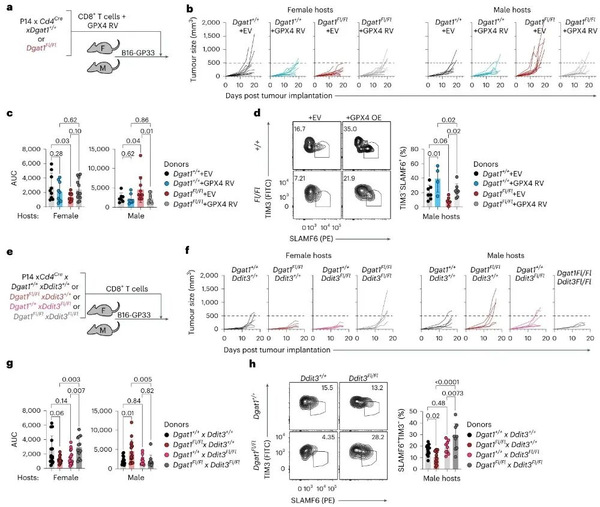
将过表达GPX4(铁死亡负调控因子)的Dgat1 KO P14细胞转移到雄性宿主后,肿瘤生长得到有效控制,祖细胞样Tₑₓ细胞频率显著升高,表明缓解脂质过氧化可补偿雄性中Dgat1的缺失;而构建Dgat1 × Ddit3双敲除P14细胞后,双敲除细胞在雄性宿主中控制肿瘤的效果与WT细胞相当,祖细胞样Tₑₓ细胞丰度增加,但在雌性宿主中,双敲除反而消除了Dgat1单敲除带来的抗肿瘤益处,提示CHOP(Ddit3编码产物)在雌性和雄性中对Dgat1 KO细胞功能的调控存在差异。