在人类与癌症的长期对抗中,治疗手段不断演进:从手术切除到放化疗,再到如今备受瞩目的免疫治疗,科技的发展为患者带来了越来越多的希望。在免疫治疗的“明星阵容”中,除了广为人知的CAR-T疗法,还有一位低调却实力非凡的“主角”——NK细胞(自然杀伤细胞)。如今,科学家正以前所未有的方式改造和武装这支天生具备抗癌潜力的“部队”,将其从人体免疫卫士转变为精准打击癌细胞的前沿力量,开启基于NK细胞的免疫治疗新时代。
NK细胞的“天赋异禀”
在我们体内的免疫大军中,NK细胞是一支与生俱来的“快速反应部队”(详细介绍见第26期科普专栏)。它的最大特点在于具备“先天智能”识别系统:无需像T细胞那样经过复杂的“培训”(即抗原预致敏),即可通过表面一系列激活性与抑制性受体的动态平衡,迅速判断“敌我”。一旦发现丢失了正常身份标识(如MHC-I分子)的癌变或感染细胞,NK细胞会立即启动杀伤程序,同时释放干扰素-γ等信号分子,拉响全身免疫警报[1]。正是这种独特的生物学能力,使得基于NK细胞的免疫疗法相较于CAR-T疗法展现出更高的安全性和更易开发为“现货型”通用药物的潜力,并保留了多重天然杀伤机制,为癌症治疗带来了全新可能。
基于NK细胞的治疗策略
目前,基于NK细胞的抗肿瘤策略主要分为以下三类:免疫检查点抑制剂、NK细胞接合器(NKCE)以及过继性NK细胞转输治疗(图1)。
1. 免疫检查点抑制剂
NK细胞表面表达多种抑制性受体,如NKG2A、TIGIT、LAG-3、TIM-3等。肿瘤细胞常利用这些受体逃避免疫攻击。通过使用单克隆抗体阻断这些“刹车”分子,可有效恢复NK细胞的抗肿瘤活性[2, 3]。例如,抗NKG2A抗体能阻断其与HLA-E的相互作用,在肺癌等多种肿瘤模型中已显示出治疗潜力[4]。
2. NK细胞接合器
NK细胞接合器是一类双/多特异性抗体样分子,能同时识别肿瘤抗原和NK细胞表面的激活受体,从而将NK细胞精准引导至肿瘤细胞附近并激活其杀伤功能。根据作用靶点的不同,主要可分为靶向CD16、NKG2D或自然细胞毒性受体(NCR)的NKCE[2]。例如,AFM13是一种能够结合NK细胞表面CD16受体与肿瘤细胞表面CD30的双特异性抗体。近期临床试验结果显示,AFM13联合NK细胞过继输注在复发或难治性淋巴瘤患者中展现出良好的疗效和安全性[5, 6]。
3. 过继性NK细胞转输治疗
该疗法通过将体外扩增、激活或经过基因改造的NK细胞作为“活性药物”输注至患者体内,以增强其抗肿瘤免疫反应。根据细胞来源,可分为自体NK细胞和异体NK细胞两种应用模式。其中,异体NK细胞因其可即时获取、抗瘤谱广且不会引发移植物抗宿主病等优势,已成为当前研发的热点。NK细胞的来源也十分丰富,包括外周血、脐带血及诱导多能干细胞(iPSC)等[7]。此外,通过基因工程为NK细胞装上“导航系统”(CAR),使其能够精准识别特定肿瘤抗原,正成为新一代NK细胞疗法的重要方向[2, 8]。
目前,上述疗法大多尚处于临床前或早期临床试验阶段,但已在部分血液肿瘤和实体瘤中初步展现出良好的安全性和一定的疗效。尤其值得注意的是,通用型和即用型NK细胞产品在产业化方面展现出巨大的潜力。尽管如此,NK细胞疗法要实现广泛临床应用,仍面临几大核心挑战:一、如何克服免疫抑制性的肿瘤微环境;二、如何提升NK细胞在体内的持久性与功能活性;三、如何实现规模化、标准化、低成本的细胞生产[2, 9]。
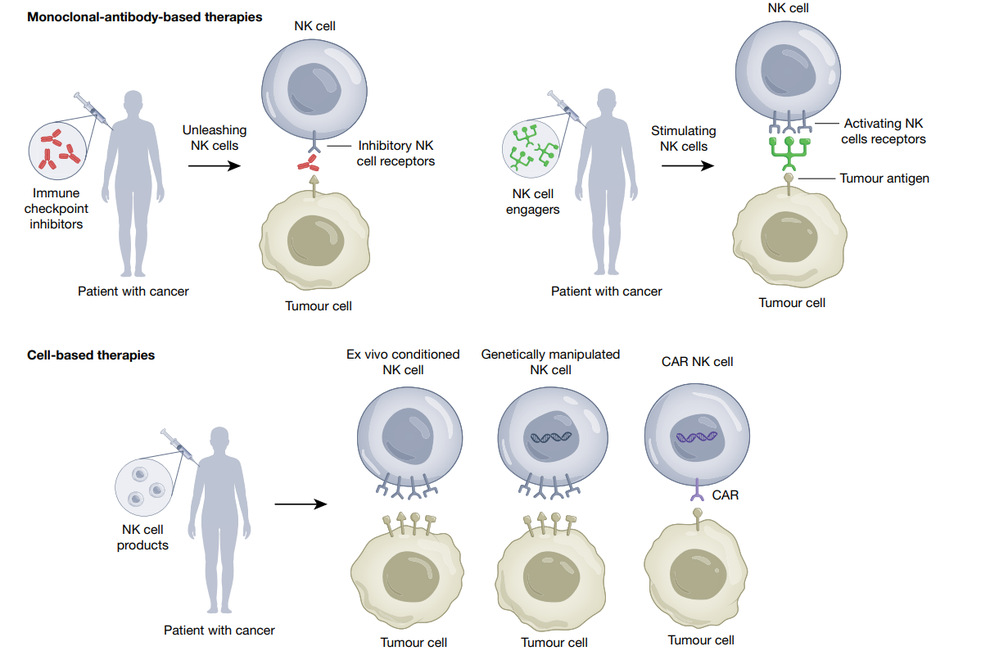
图1 基于NK细胞的肿瘤治疗策略[2]
总结与展望
NK细胞凭借其天然识别能力和低毒性优势,正成为免疫治疗领域中备受关注的研究热点。通过免疫检查点抑制剂、NK细胞接合器、过继性NK细胞输注(包括CAR-NK)等多路径探索,科学家正逐步推动该疗法从血液肿瘤向实体瘤拓展。未来,NK细胞疗法的突破将依赖于对NK细胞生物学机制的深入理解、基因工程技术的不断进步以及更为精准的联合治疗方案设计。
彭慧课题组供稿
参考文献
1.Wolf, N.K., D.U. Kissiov, and D.H. Raulet, Roles of natural killer cells in immunity to cancer, and applications to immunotherapy. Nat Rev Immunol, 2023. 23(2): p. 90-105.
2.Vivier, E., et al., Natural killer cell therapies. Nature, 2024. 626(8000): p. 727-736.
3.Zhang, Q., et al., Blockade of the checkpoint receptor TIGIT prevents NK cell exhaustion and elicits potent anti-tumor immunity. Nat Immunol, 2018. 19(7): p. 723-732.
4.Andre, P., et al., Anti-NKG2A mAb Is a Checkpoint Inhibitor that Promotes Anti-tumor Immunity by Unleashing Both T and NK Cells. Cell, 2018. 175(7): p. 1731-1743 e13.
5.Nieto, Y., et al., Allogeneic NK cells with a bispecific innate cell engager in refractory relapsed lymphoma: a phase 1 trial. Nat Med, 2025. 31(6): p. 1987-1993.
6.Kim, W.S., et al., A Phase II Study of Acimtamig (AFM13) in Patients with CD30-Positive, Relapsed, or Refractory Peripheral T-cell Lymphomas. Clin Cancer Res, 2025. 31(1): p. 65-73.
7.Myers, J.A. and J.S. Miller, Exploring the NK cell platform for cancer immunotherapy. Nat Rev Clin Oncol, 2021. 18(2): p. 85-100.
8.Liu, E., et al., Use of CAR-Transduced Natural Killer Cells in CD19-Positive Lymphoid Tumors. N Engl J Med, 2020. 382(6): p. 545-553.
9.Bald, T., et al., The NK cell-cancer cycle: advances and new challenges in NK cell-based immunotherapies. Nat Immunol, 2020. 21(8): p. 835-847.
