科学家以黑腹果蝇为模式生物,持续探索着天然免疫的分子面纱。这一物种凭其遗传背景纯粹、信号通路保守的先天免疫网络,将微观基因型与宏观表型精准耦合为可定向操控的因果链。加之其基因组小、繁殖快、75%人类疾病基因可同源建模,使疾病相关免疫逃逸机制得以在活体水平快速建模与高通量筛选,从而成为天然免疫研究不可替代的精灵。
法国科学家朱尔斯·霍夫曼(Jules A. Hoffmann)在一次偶然的实验中注意到,少数果蝇被真菌感染后全身布满菌丝(图1),而绝大多数果蝇却能存活。进一步研究发现,Toll基因突变阻断了感染信号诱导抗菌肽的表达,使果蝇丧失对细菌和真菌的抵抗力。霍夫曼团队以果蝇为模型,首次证明Toll基因在识别病原体、启动天然免疫中的核心作用,并因此荣获2011年诺贝尔生理学或医学奖。小小的果蝇助推免疫学跨越式前进,也让黑腹果蝇成为第五次帮助科学家问鼎诺奖的明星模型。这一发现揭示了天然免疫系统的古老起源,也促使科学家重新审视其在进化中的保守性与重要性。
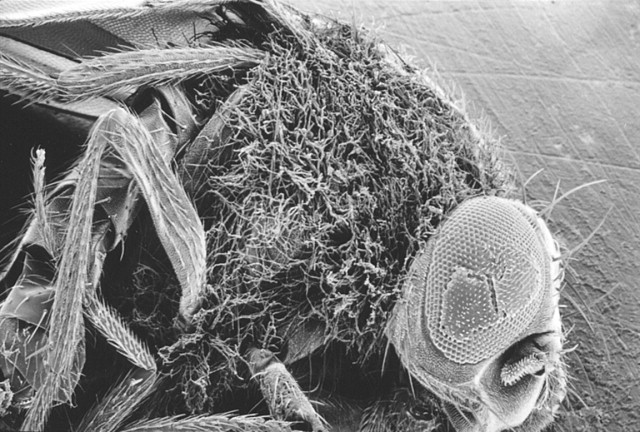
图1. 敲除Toll基因的果蝇死于真菌感染[1]
古老保守且重要的天然免疫系统
从进化视角看,疾病是与生命相伴相生的古老生物学现象。其主要包括感染性疾病(真菌、细菌、病毒)与非感染性疾病(肿瘤)。前者源于病原与宿主对资源的持续争夺;后者则来自物理、化学或代谢胁迫。二者共同构成生命体恒常的选择压力。为应对此双重挑战,生命体也自然演化出同样古老的先天免疫系统,作为机体的第一道免疫防线。天然免疫系统,也被称作非特异性免疫系统(Non-specific immune system),是一种十分重要的免疫机制,其在基因、分子和机制等层面高度保守。
果蝇纯粹的天然免疫体系
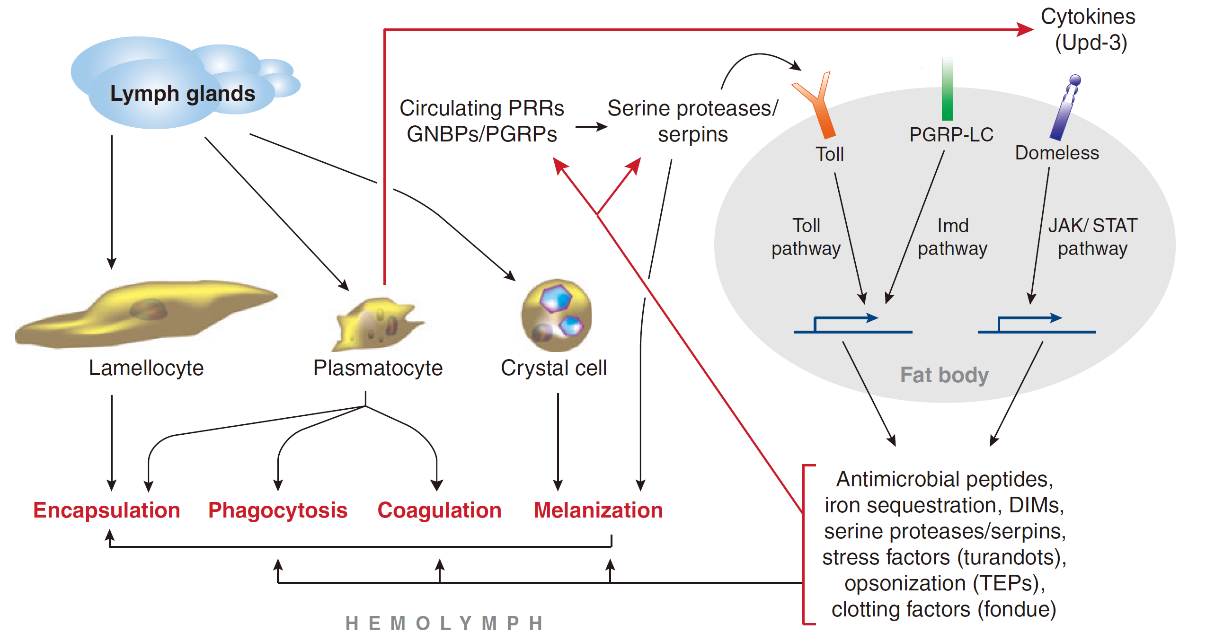
图2 果蝇先天免疫防御体系[2]
果蝇的先天性免疫防御反应,主要包括细胞免疫和体液免疫。果蝇的血细胞包括浆细胞(plasmatocytes)、晶细胞(crystal cells)和薄层细胞(lamellocytes),分别参与吞噬和促进伤口愈合、介导黑化反应(melanization)、包裹大型病原体等功能[3]。果蝇的细胞免疫发生于血腔中,主要涉及血细胞的增殖、分化、迁移、黏附和延展。而体液免疫则涉及黑化反应、Toll、Imd、Jak/Stat和ROS免疫反应通路以及抗菌肽和应激因子的分泌。Toll/IMD通路的激活都是通过识别细菌表面的肽聚糖而实现的,不同的肽聚糖识别受体(Peptidoglycan recognition proteins ,PGRP)识别来源于不同种类细菌的肽聚糖,从而具有了一定的特异性。它们的激活能够导致不同的核转录因子NF-κB家族成员的入核,从而导致下游基因,例如抗菌肽的表达[2, 3]。果蝇的天然免疫系统和发育机制与哺乳动物高度保守。由于果蝇缺乏T细胞、B细胞等适应性免疫组分,天然免疫成为其抵御病原体的唯一防线。这一优势排除了获得性免疫的交叉干扰,使得果蝇成为天然免疫领域的“万能钥匙”。
果蝇疾病模型
为阐明疾病背后的致病机制并开发防治策略,科学家建立了多种动物模型。黑腹果蝇因缺乏获得性免疫的“干扰”,宿主先天防御的对抗被放大、简化,成为研究疾病进展的独特窗口;借此优势,果蝇感染及非感染模型应运而生。
果蝇感染模型已被广泛用于解析多种病原的致病机制及宿主免疫防御策略。它不仅帮助解析了通过伤口传播的绿脓杆菌(Pseudomonas aeruginosa)的毒力因子[4],还证实了促凋亡信号通路在鼠伤寒沙门氏菌(Salmonella Typhimurium)所致严重腹泻中的调控效应[5]。此外引发肺炎的金黄色葡萄球菌(Staphylococcus aureus)[6]及威胁孕妇和儿童健康的李斯特菌(Listeria monocytogenes)也均可用果蝇造模。
除了细菌和前文提到的真菌,病毒也可借助果蝇造模。借助果蝇模型可以阐明长新冠患者为何持续腹泻[7]。此外,鉴于果蝇在进化上的分类与蚊子十分接近,以及果蝇的免疫系统、生理习性与蚊子有较强的保守性,果蝇感染模型为研究虫媒病毒传播提供了良好的平台,如大家熟知的登革病毒(dengue virus, DENV)[8]、寨卡病毒(Zika virus, ZIKV)[9]、西尼罗病毒(West Nile virus, WNV)[10]、辛德毕斯病毒(Sindbis virus, SinV)[11]和基孔肯雅病毒(Chikungunya virus, CHIKV)[12]等由蚊虫传播的人畜共患病病毒,都可以在果蝇上进行感染模拟。
癌症现在已成为人类健康的最主要敌人之一,而且随着人类寿命的不断延长,患癌的风险也随之增高。果蝇是怎样与癌症研究联系起来的?很多与生长调控有关的信号通路,都是最先在果蝇上发现的。近年来,大规模基因组测序和功能基因组研究发现,与人类癌症相关的基因同样在果蝇中存在,并起着重要的作用,其调控异常在果蝇和人体内都可能导致肿瘤的发生。果蝇肿瘤也可分为两类,即类似于人类良性肿瘤的增生性肿瘤(hyperplastic tumor)和类似于人类恶性肿瘤的赘生性肿瘤(neoplastic tumor)。一系列研究表明,果蝇作为一种经典的模式生物也可以用来研究癌症转移[13]、微环境[14]、癌性恶液质[15]和副肿瘤综合征[16]
果蝇强大的筛选体系
果蝇拥有成熟的基因编辑工具,如CRISPR-Cas9、Gal4/UAS系统等。这些工具可精准敲除、敲入或调控特定基因表达,便于构建疾病模型或研究基因功能。例如,通过Gal4/UAS系统可在特定组织或细胞中特异性表达或抑制基因,实现对基因功能的时空控制。
与此同时,果蝇基因组保守性高。果蝇约75%的人类疾病相关基因在果蝇中存在同源基因,且基因功能和调控机制高度保守。这使得果蝇成为研究人类疾病机制、药物靶点发现和功能基因筛选的理想模型,许多在果蝇中发现的基因功能和通路在人类中具有相似作用。
此外,利用果蝇进行模型筛选具有效率高的突出优势。果蝇繁殖周期短(10-12天)、繁殖能力强,可在短时间内产生大量后代,便于进行大规模遗传筛选。与此同时,果蝇具有丰富的表型特征,如发育畸形、行为异常、代谢变化等,可通过简单直观的方法进行筛选。例如,通过观察果蝇的运动能力、学习记忆能力、寿命等表型,可快速评估基因功能或药物效果。加之果蝇可模拟多种人类疾病,如神经退行性疾病(阿尔茨海默病、帕金森病)、肿瘤、代谢性疾病(糖尿病、肥胖)、炎症性疾病等。这些疾病模型为研究疾病机制、筛选治疗药物和验证药物靶点提供了有力工具。
结束语
正如霍夫曼教授在访谈中强调的:“黑腹果蝇的价值不仅在于它揭示了过去,更在于它指引着未来。”这枚振翅即生风的小精灵,仍在源源不断地点燃人类破解免疫奥秘、攻克疾病的灵感星火。
潘磊课题组供稿
参考文献
1.Lemaitre, B., et al., The dorsoventral regulatory gene cassette spatzle/Toll/cactus controls the potent antifungal response in Drosophila adults. Cell, 1996. 86(6): p. 973-83.
2.Yang, S., et al., Sugar Alcohols of Polyol Pathway Serve as Alarmins to Mediate Local-Systemic Innate Immune Communication in Drosophila. Cell Host Microbe, 2019. 26(2): p. 240-251 e8.
3.Lemaitre, B. and J. Hoffmann, The host defense of Drosophila melanogaster. Annu Rev Immunol, 2007. 25: p. 697-743.
4.Martinez, E. and J. Campos-Gomez, Oxylipins produced by Pseudomonas aeruginosa promote biofilm formation and virulence. Nat Commun, 2016. 7: p. 13823.
5.Frandsen, J.L., et al., Salmonella pathogenesis reveals that BMP signaling regulates blood cell homeostasis and immune responses in Drosophila. Proc Natl Acad Sci U S A, 2008. 105(39): p. 14952-7.
6.Needham, A.J., et al., Drosophila melanogaster as a model host for Staphylococcus aureus infection. Microbiology (Reading), 2004. 150(Pt 7): p. 2347-2355.
7.Wang, M., et al., Impaired VLCFA-peroxisome-mediated intestinal epithelial repair causes gastrointestinal sequelae of long COVID. Dev Cell, 2026.
8.Sessions, O.M., et al., Discovery of insect and human dengue virus host factors. Nature, 2009. 458(7241): p. 1047-50.
9.Eleftherianos, I. and S. Mallick, Drosophila-Zika virus interactions: Dissecting host immunity and pathology against flavivirus infection. Virology, 2025. 610: p. 110603.
10.Mead, E.B., et al., Drosophila melanogaster Limostatin and Its Human Ortholog Promote West Nile Virus Infection. Insects, 2024. 15(6).
11.Mudiganti, U., et al., Sindbis virus infection of two model insect cell systems--a comparative study. Virus Res, 2006. 122(1-2): p. 28-34.
12.McFarlane, M., et al., Characterization of Aedes aegypti innate-immune pathways that limit Chikungunya virus replication. PLoS Negl Trop Dis, 2014. 8(7): p. e2994.
13.Kong, D., et al., Adipose tissue-secreted Spz5 promotes distal tumor progression via Toll-6-mediated Hh pathway activation in Drosophila. EMBO J, 2025. 44(15): p. 4301-4330.
14.Katheder, N.S., et al., Microenvironmental autophagy promotes tumour growth. Nature, 2017. 541(7637): p. 417-420.
15.Liu, Y., et al., Hepatic gluconeogenesis and PDK3 upregulation drive cancer cachexia in flies and mice. Nat Metab, 2025. 7(4): p. 823-841.
16.Kwok, S.H., et al., Paraneoplastic renal dysfunction in fly cancer models driven by inflammatory activation of stem cells. Proc Natl Acad Sci U S A, 2024. 121(42): p. e2405860121.
