骨科植入物相关感染(Implant-related infections, IRIs)是骨科、齿科等领域面临的重大临床挑战。其核心病理在于,细菌生物膜的形成不仅引发过度炎症、破坏骨组织,更会系统性排斥并功能抑制骨髓间充质干细胞(BMSCs),致使植入界面陷入“感染持续-再生受阻”的恶性循环。传统抗菌涂层与载药策略多属“补偿性”治疗,致力于通过外源性药物清除病原、调节免疫,却难以逆转干细胞的功能抑制状态,导致骨整合失败。
3月28日,免疫应答与免疫治疗全国重点实验室朱晨教授团队在顶级期刊发表最新研究成果,开发了一种pH响应型金属-酚配位智能涂层(DPMg@DM),实现了从“被动载药”到“主动细胞重编程”的根本性跨越。该涂层能精准响应感染微环境的酸度变化,顺序释放抗菌肽(DOPA-MLT)与免疫调节性镁离子(Mg²⁺),同时稳固展示干细胞靶向肽(DOPA-PFS),以协同完成感染控制、免疫调控及细胞招募。
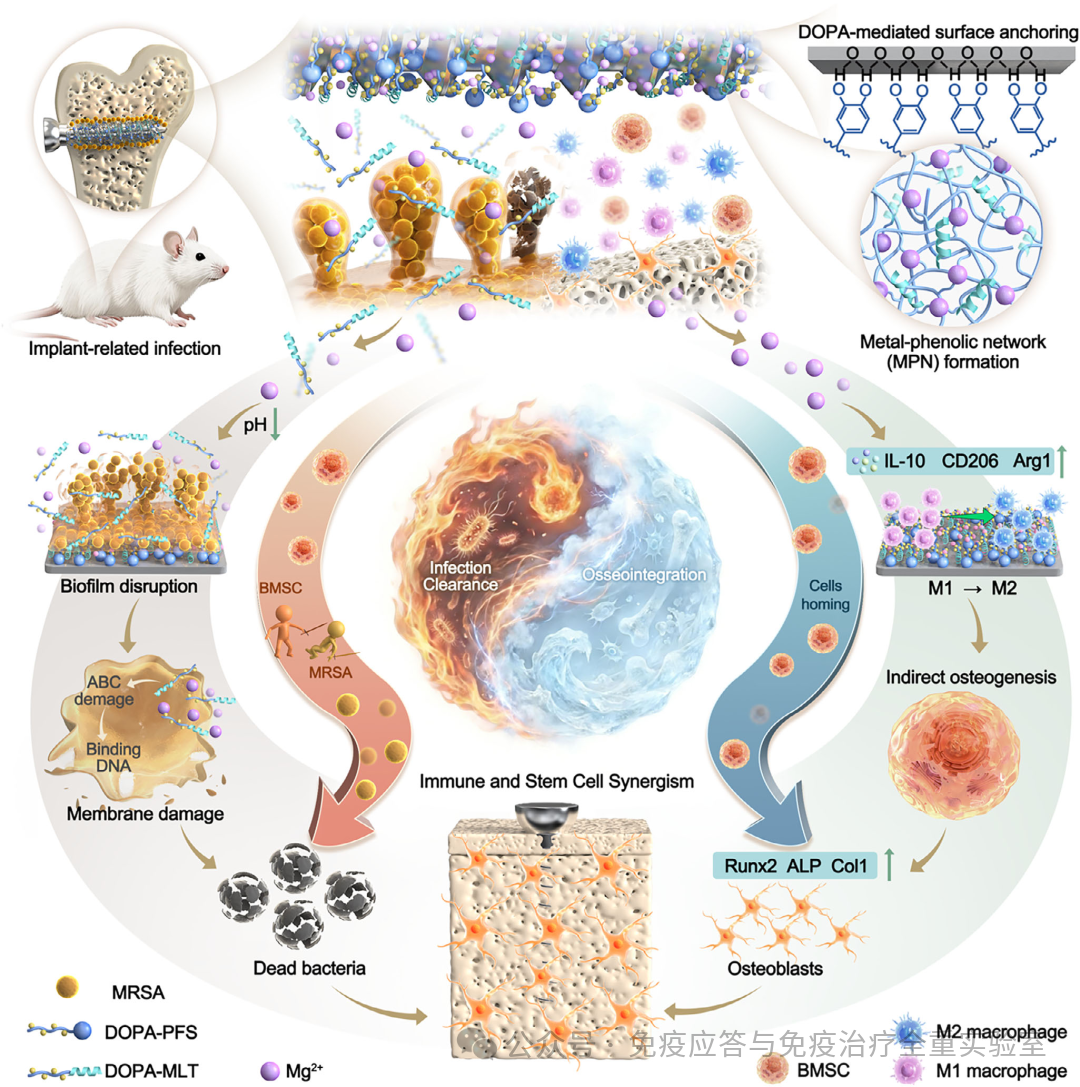
方案1 受贻贝启发的涂层通过金属-酚醛配位作用在钛植入物示意图
1. 主要研究
1.1 制备与表征
该智能涂层通过贻贝启发的金属-酚配位化学在钛表面制备。其核心是一个三步自组装过程:首先将钛基底依次浸泡在含干细胞靶向肽(DOPA-PFS)、镁离子(Mg²⁺)和抗菌肽(DOPA-MLT)的溶液中,Mg²⁺作为交联中心,与两种肽上的DOPA基团配位,形成稳定的网络涂层。表征结果显示,该涂层显著改变了材料表面特性:AFM表明其表面形貌变得复杂且粗糙度增加,接触角测量显示表面从疏水性转变为亲水性,XPS证实了碳、氮元素含量上升及肽键特征峰的出现,UV-vis光谱在280nm处的强吸收峰证实了金属-酚配位网络的形成。关键的是,ICP-MS测定的释放实验证明该系统具有pH响应性:在生理pH下Mg²⁺释放缓慢而稳定,而在模拟感染环境的酸性条件下则会快速释放,实现了针对病理微环境的智能响应。
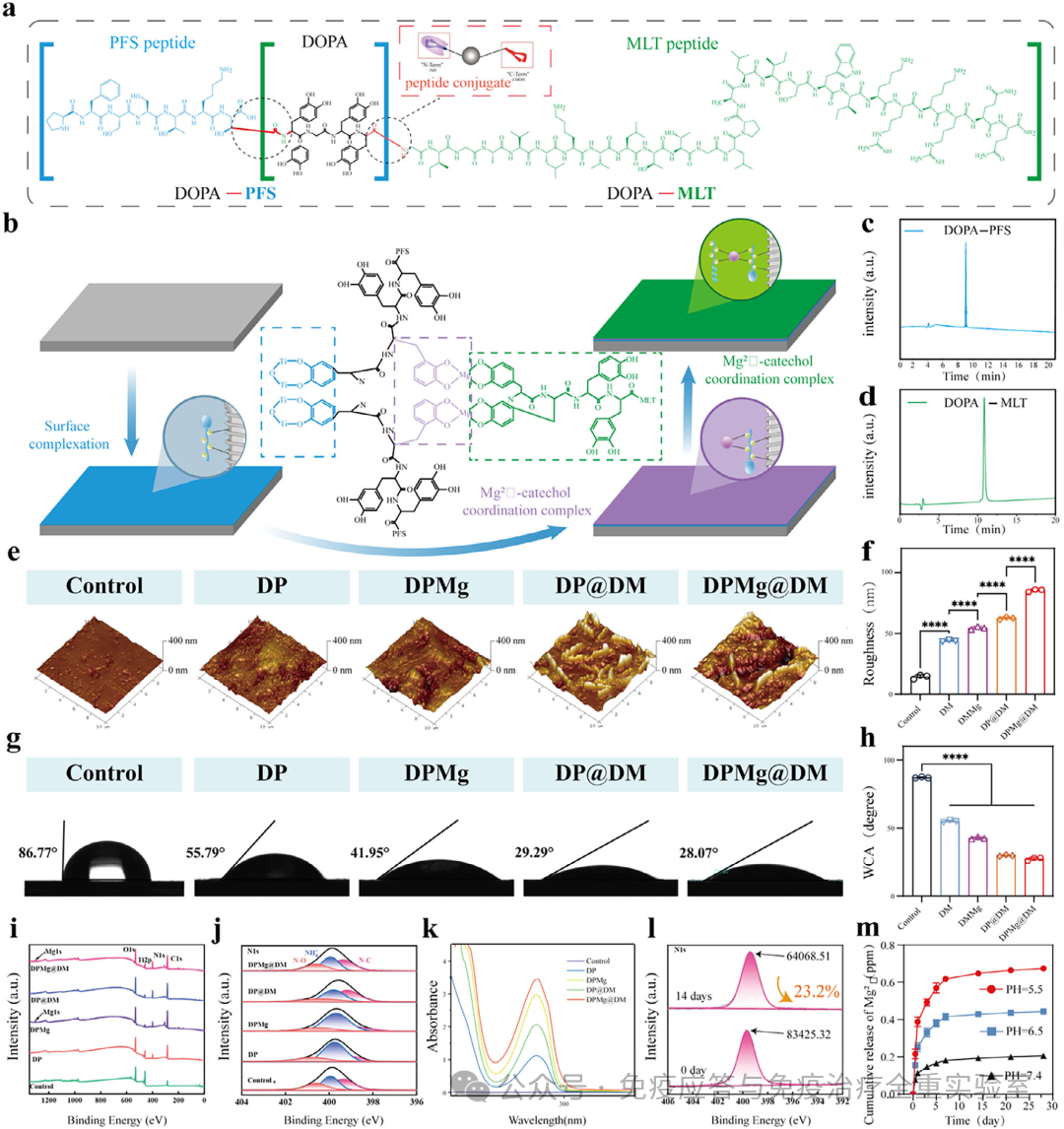
图1 制备与表征
1.2 抑菌性能研究
研究针对两种临床常见病原体(大肠杆菌和耐甲氧西林金黄色葡萄球菌MRSA),从预防生物膜形成和清除浮游细菌两个维度进行了测试。结果表明,该涂层能显著抑制生物膜的形成(晶体紫染色与3D共聚焦显微镜显示生物膜生物量与厚度均大幅减少),并能高效杀灭浮游细菌。流式细胞术定量分析进一步证实,涂层表面细菌死亡率极高(大肠杆菌达81.5%,MRSA达65.4%)。这些数据综合证明,该多功能涂层能通过双重机制提供强大而全面的抗菌保护。
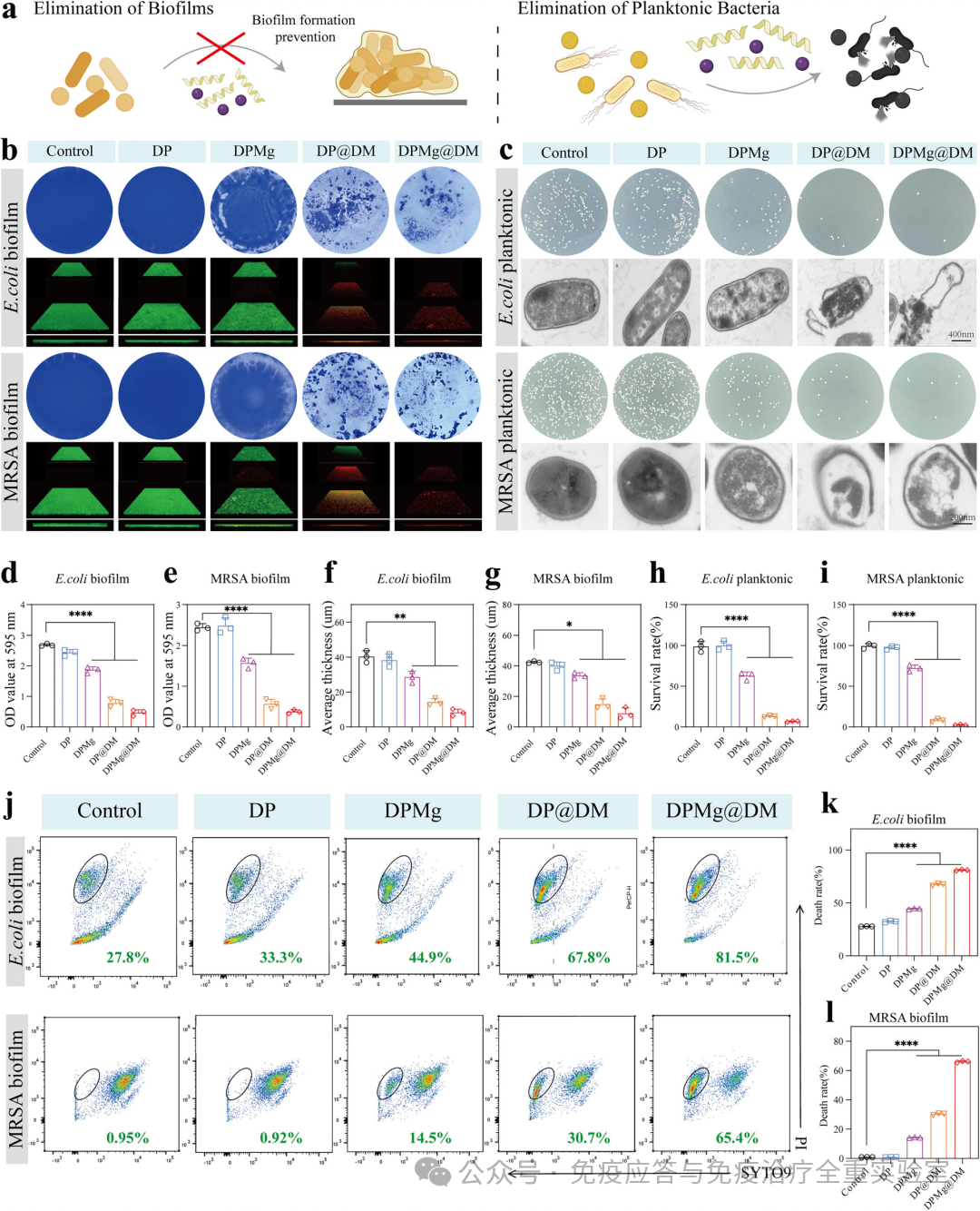
图2 抑菌性能研究
1.3 转录组学与功能实验
转录组分析显示,涂层处理能广泛重编程细菌(MRSA)的基因表达,显著下调与群体感应、磷酸转移酶系统、ATP结合盒转运蛋白及细菌分泌系统相关的基因。基因集富集分析(GSEA)进一步证实,涂层能系统性抑制细菌的毒力、膜相关功能及营养获取途径。功能验证表明,关键毒力基因(如agrA、abcA、ptsH)表达被显著抑制,同时细菌膜蛋白泄漏和膜通透性增加。扫描电子显微镜(SEM)直观地展示了涂层处理导致的细菌严重形态损伤。这些结果共同表明,该涂层的抗菌作用超越了简单的膜破坏,是通过干扰细菌的关键生理与通讯系统,引发其系统性的代谢与结构崩溃来实现的。
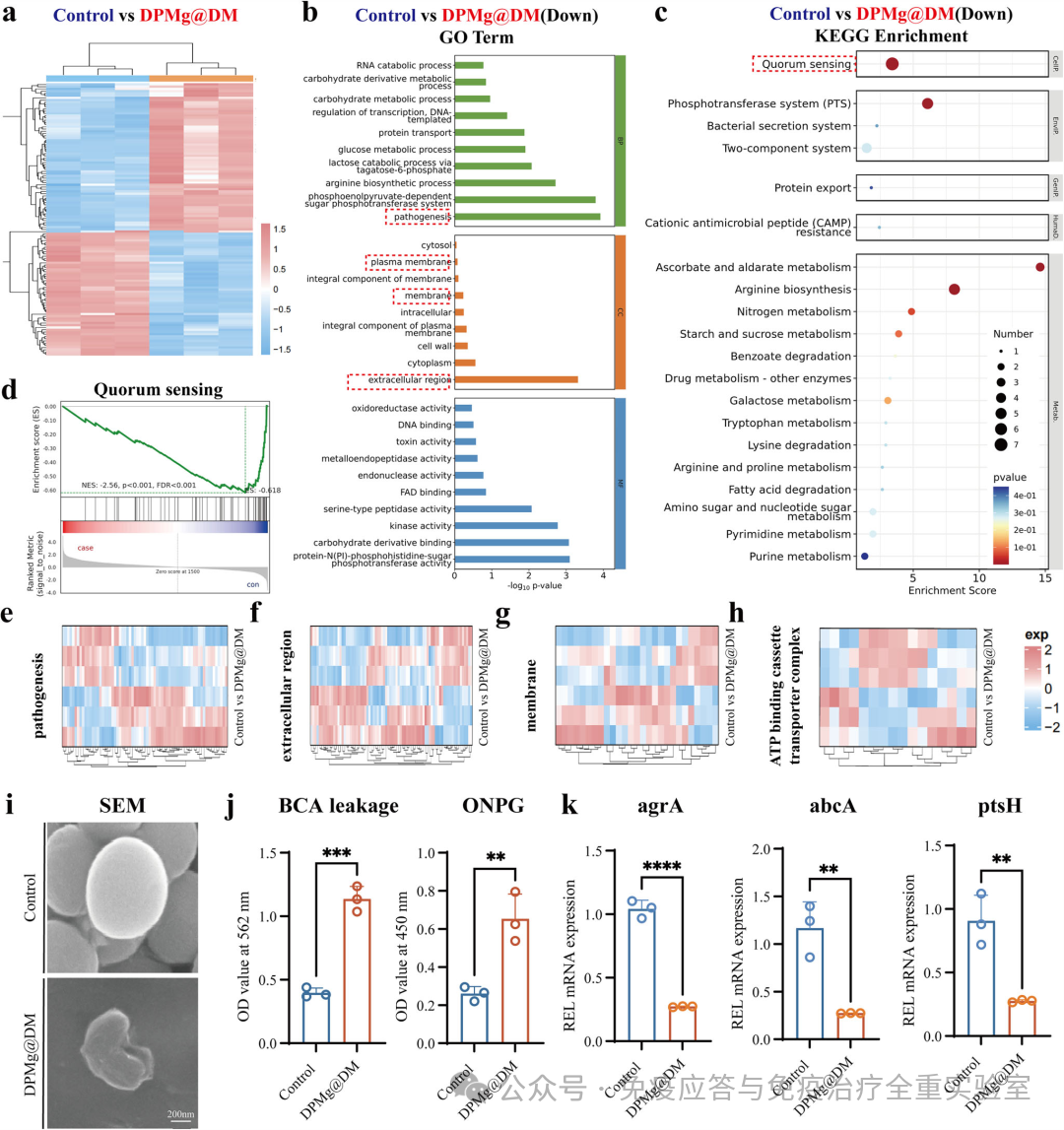
图3 转录组学与功能实验
1.4 调控免疫微环境的核心机制
研究聚焦于巨噬细胞表型极化,发现镁离子能驱动巨噬细胞从促炎、破坏性的M1型向促修复、抗炎的M2型转化。免疫荧光与流式细胞术定量显示,含镁涂层(DPMg和DPMg@DM)表面M1巨噬细胞比例显著降低,而M2巨噬细胞比例大幅升高,其中DPMg@DM组效果最为显著(M1比例从对照的59.6%降至19.4%)。RNA测序与通路分析从分子层面揭示了其作用机理:镁处理引发了巨噬细胞广泛的转录重编程,并特异性抑制了NOD样受体、IL-17等关键促炎信号通路。这证实了涂层能够主动将感染部位的免疫反应从“破坏模式”切换至“修复模式”,为后续干细胞介导的骨再生创造了必需的抗炎微环境。
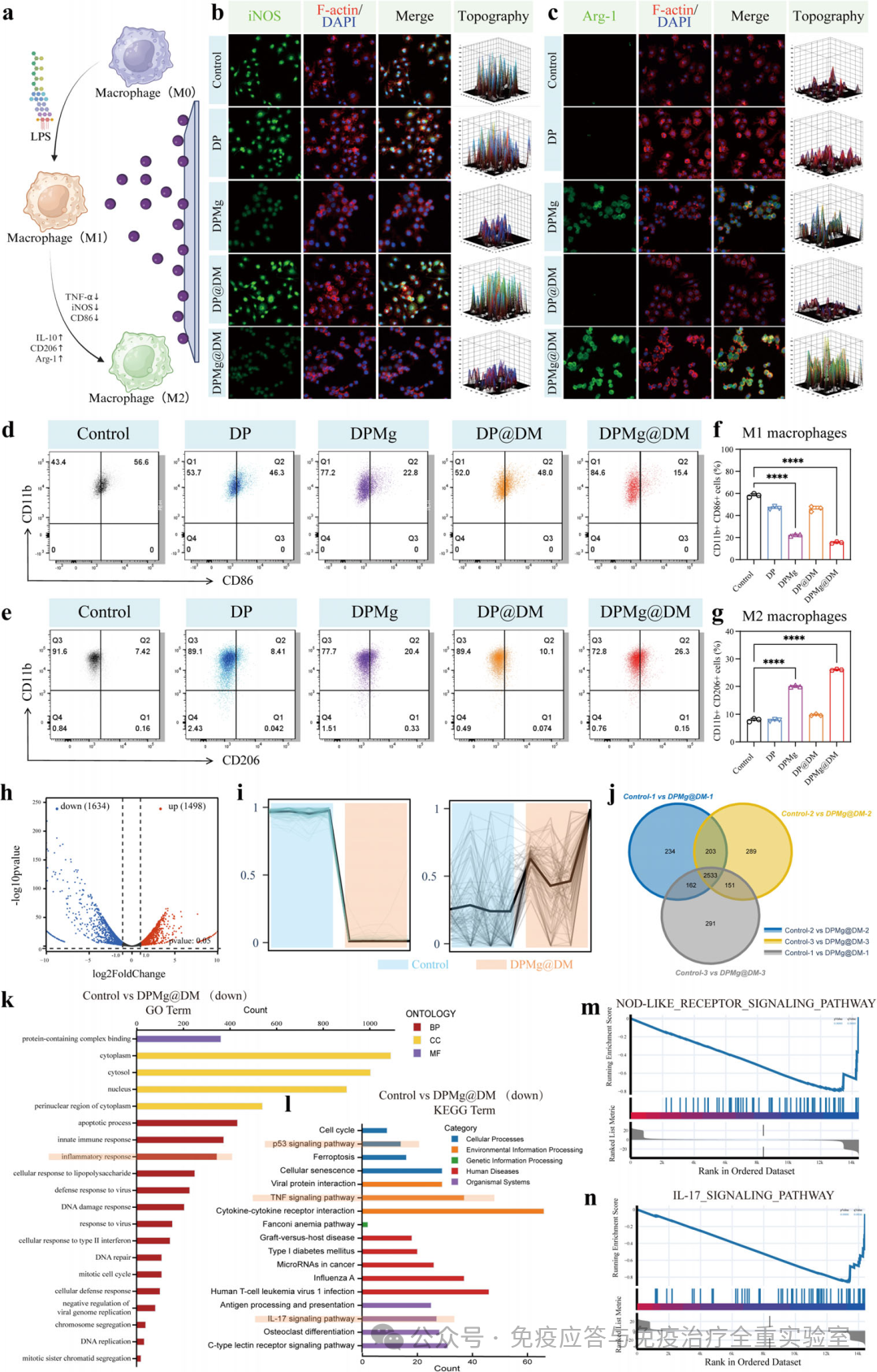
图4 调控免疫微环境的核心机制
1.5 干细胞层面的核心治疗机制
涂层通过DOPA-PFS肽有效招募BMSCs至材料表面,而释放的镁离子(Mg²⁺)则激活了BMSCs内的Wnt/β-catenin信号通路(Western blot显示β-catenin核转位)。这一通路激活同时上调了成骨基因(如RUNX2, OCN)和抗菌效应程序。关键证据来自竞争性共培养实验:在涂层上,BMSCs能显著抑制MRSA和大肠杆菌的定植,而普通钛表面则被细菌主导。此外,经涂层激活的BMSCs的培养上清也显示出抗菌活性。转录组学分析进一步确认了Wnt通路的核心协调作用。这些发现证明,该涂层将干细胞从被动的“修复者”重编程为主动参与感染清除与骨再生的治疗主体,实现了治疗范式的根本转变。
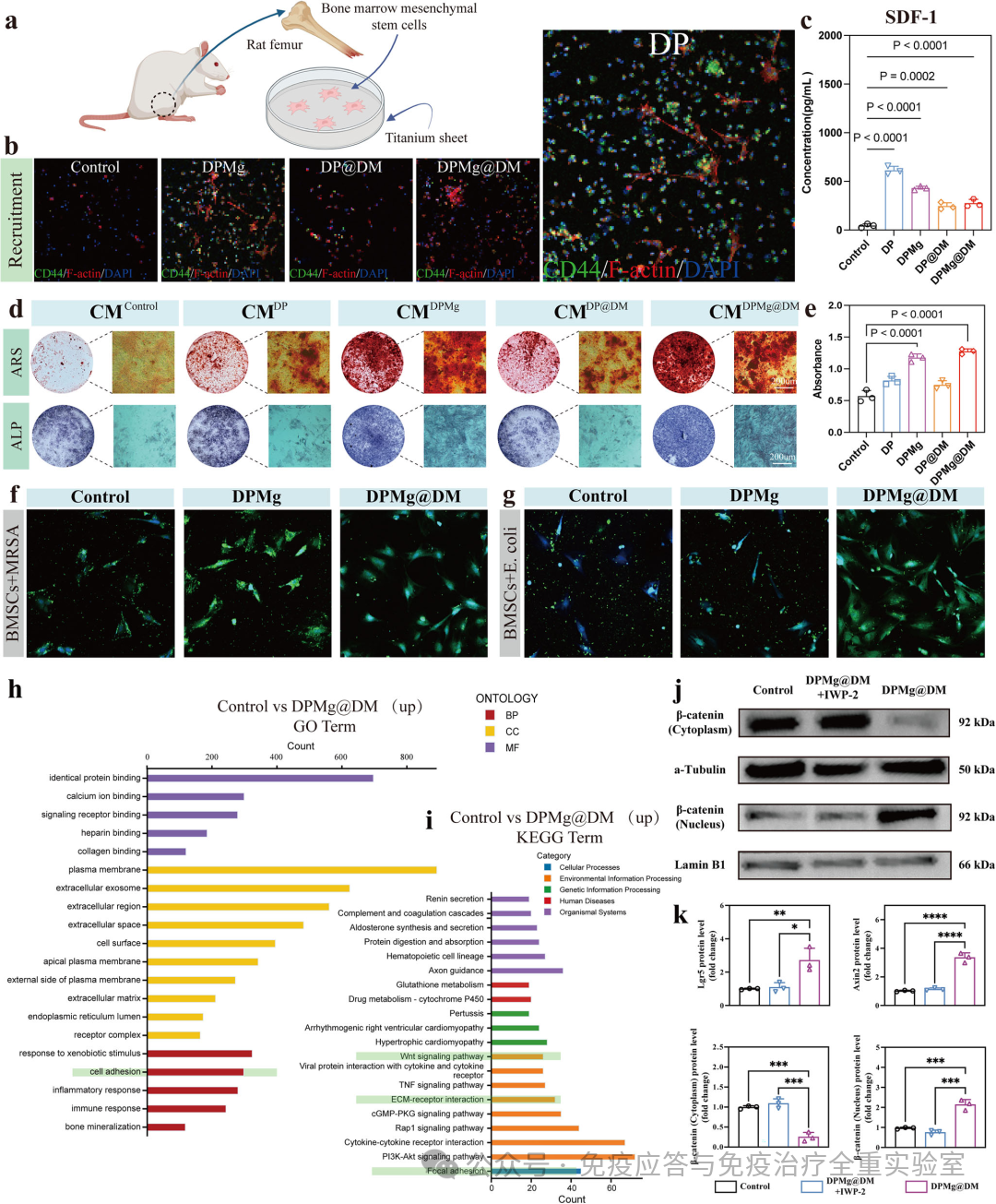
图5 干细胞层面的核心治疗机制
1.6 大鼠股骨植入物MRSA感染模型
通过系统的体内实验,在大鼠股骨植入物MRSA感染模型中,完整验证了该智能涂层的时序性协同治疗效能。研究显示,在植入早期(第7天),涂层能实现超过4个数量级的细菌杀灭,有效清除生物膜并控制急性炎症;在中期(第14天),它成功将病灶区的巨噬细胞从促炎的M1型极化为促修复的M2型,建立了有利于再生的免疫微环境;最终,在长期(第8周)评估中,涂层驱动了显著的骨再生与整合,使植入体-骨界面处的骨体积(BV/TV)相比对照组提升了280%,并显著改善了骨矿物质密度与骨小梁结构。这些结果综合证实,该涂层能按“清除感染-调节免疫-促进再生”的时序逻辑,协同解决植入物感染难题,并实现卓越的骨整合效果。
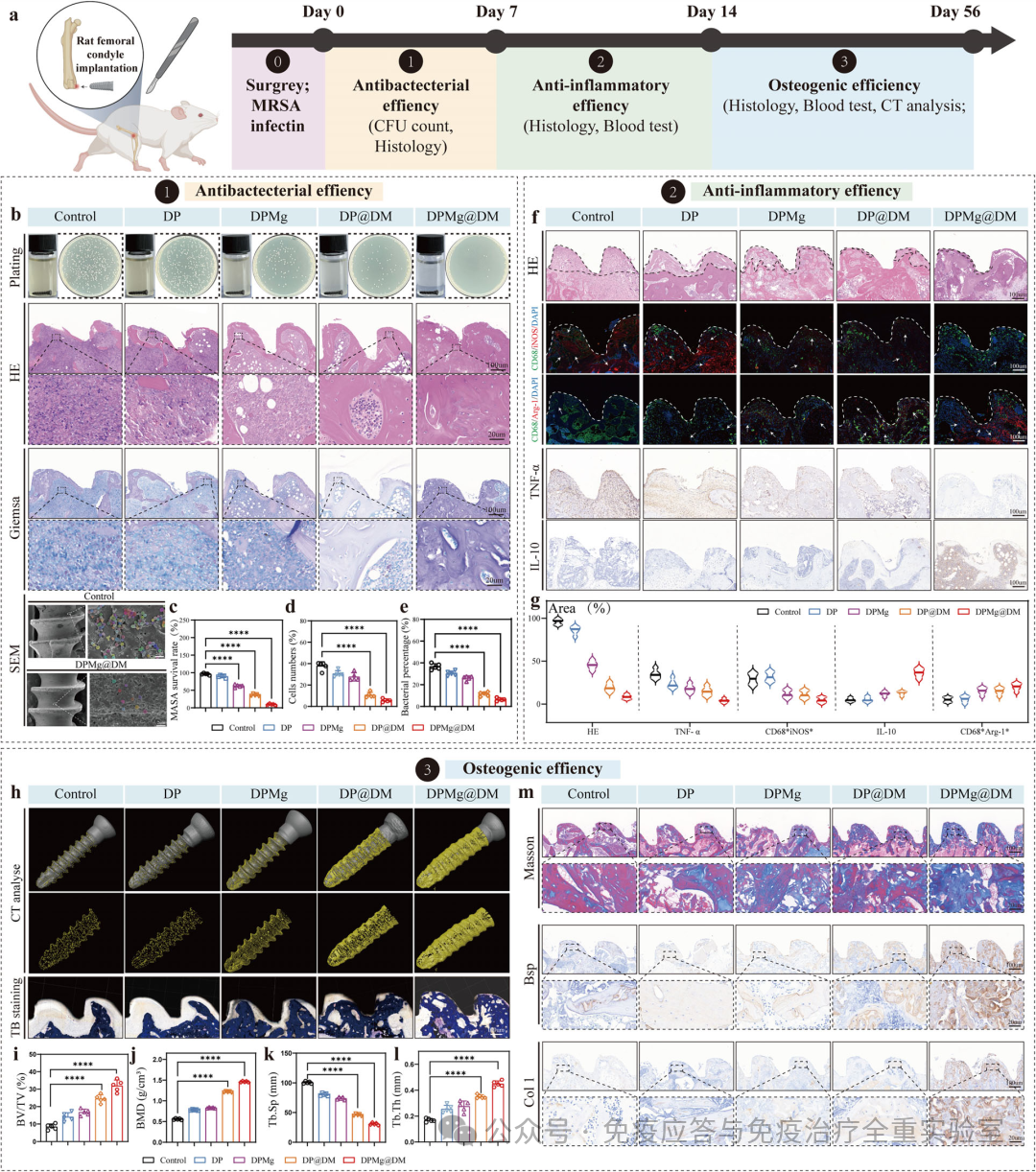
图6 大鼠股骨植入物MRSA感染模型
2. 总结
本研究最显著的创新在于,该涂层能够将招募至病灶的BMSCs“重编程”为具备双重功能的治疗主体。机制上,镁离子激活了BMSCs中经典的Wnt/β-catenin信号通路,从而同时解锁了其内在的抗菌效应程序与高效的成骨分化程序。这意味着,干细胞不再仅是需被保护的修复细胞,而是被赋能成为兼具“杀菌”与“成骨”能力的主动治疗者。动物模型验证了该策略的强大效力:在大鼠股骨植入物MRSA感染模型中,该涂层实现了>4个数量级的细菌杀灭,并驱动界面骨体积显著提升280%。这项工作不仅展示了一种高效协同抗感染与促再生的新型生物材料,更从理念上革新了植入器械的设计逻辑——即通过智能材料调控内源性干细胞命运,将其转化为对抗疾病、促进修复的“活体治疗药剂”,为解决植入物感染这一顽固临床难题开辟了全新的道路。
原文链接:https://doi.org/10.1002/adma.72941
