近日,免疫应答与免疫治疗全国重点实验室王育才教授团队在国际顶级化学期刊发表最新研究成果,。
mRNA药物发展的核心挑战仍然是递送
近年来,mRNA技术在体内CAR-T、肿瘤免疫治疗、预防疫苗和基因编辑领域取得了快速发展。然而,。目前广泛使用的脂质纳米颗粒(LNP)在静脉给药后通常呈现明显的肝脏富集效应,这在一定程度上限制了mRNA药物在肺部疾病、免疫疾病以及肿瘤治疗等领域的应用。
如何实现mRNA药物在体内的器官和细胞选择性递送,是mRNA治疗技术进入下一阶段发展的关键问题。针对这一挑战,。该体系通过聚合物与脂质材料的协同结构设,显著拓展了纳米颗粒组成调控空间,使mRNA递送系统能够实现更灵活的器官选择。更重要的是,研究团队将设计实验与回归模型分析引入纳米递送系统开发,只需通过少量代表性配方实验,就可以建立起纳米颗粒组成与体内器官递送之间的定量预测模型。
这一方法一改传统依赖大量试错筛选的开发方式,继而转变为数据驱动的可预测设计模式。
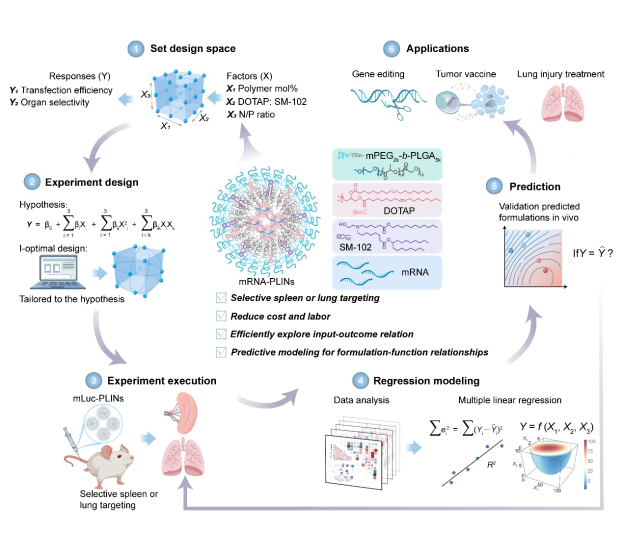
图1 采用I-optimal实验设计(DOE)框架构建模块化聚合物-脂质整合纳米颗粒(PLIN)平台,实现器官特异性mRNA递送的整体示意图
基于该模型,研究团队成功设计出多种具有显著器官靶向特性的纳米递送体系。在体内实验中,所设计的纳米颗粒能够实现:
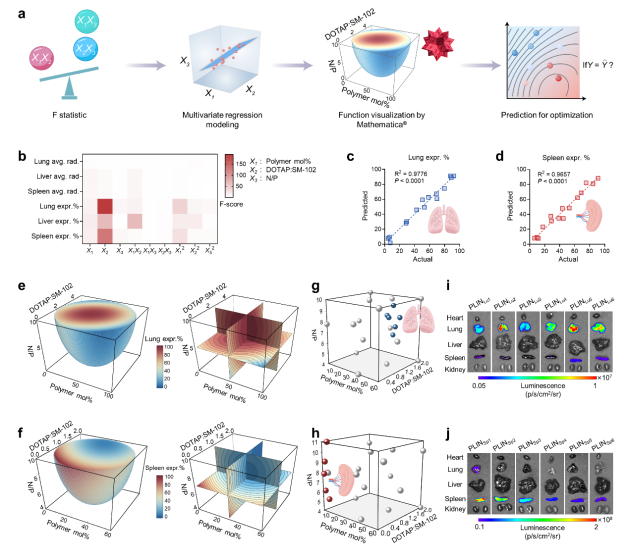
图2 回归模型指导下的器官选择性优化
为了验证该平台的应用价值,研究团队在多个疾病模型中进行了功能验证。
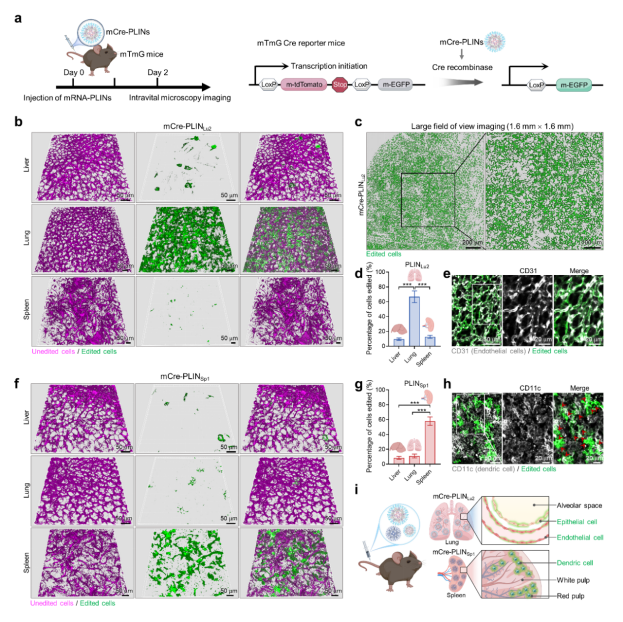
图3 器官选择性mRNA-PLIN实现肺或脾脏中的Cre介导基因编辑
随着mRNA药物不断拓展新的治疗领域,。此次研究提出的数据驱动设计框架,为mRNA递送系统的开发提供了新的工程化路径,。
