5月16日,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗全国重点实验室傅斌清教授组与魏海明教授组在Cell Press旗下免疫学期刊《Immunity》上发表了题为《Maternal natural killer cells drive neuroimmune disorders in offspring through aberrant secretion of extracellular granzyme B》的研究论文。研究发现孕期病毒感染引起母体免疫异常激活(MIA),诱导母胎界面蜕膜自然杀伤(natural killer, NK)细胞发生炎症性转变,导致胚胎大脑巨噬细胞异常活化,从而引发后代神经发育障碍以及自闭症样行为。这一突破性发现揭示了孕期母体病毒感染诱导子代神经发育异常的全新机制,建立了母胎界面免疫细胞对子代脑神经免疫调控的桥梁,对预防和治疗神经发育相关疾病具有重要的意义。

自闭症谱系障碍(autism spectrum disorder, ASD)是一种常见的神经发育障碍性疾病,病因复杂,受遗传和环境因素多重交叉影响。流行病学证据显示,孕期母体病毒感染与后代神经发育障碍和精神疾病的风险增加有关,动物模型也表明母体免疫激活可引起子代产生明显神经病理损伤及行为异常。因此,妊娠期间母体健康状况对子代健康与否具有重要影响。在妊娠过程中,母胎界面包括母体蜕膜和胎儿胎盘,是母胎互作的核心场所。其中,蜕膜NK细胞是母胎界面占主导地位的免疫细胞群体,在正常妊娠中NK细胞起到维持免疫耐受,促进螺旋动脉重塑及胎儿生长发育等重要作用。母胎界面 NK 细胞功能的异常,通常会导致不良妊娠结局的发生。
为了探究蜕膜NK细胞在孕期病毒感染相关的子代神经发育障碍中的作用,研究团队模拟病毒感染构建了小鼠MIA模型,并在孕中期使用NK细胞清除抗体处理孕鼠,通过对胎脑进行组织学检测以及后代的行为学测试,发现清除母体NK细胞明显缓解MIA导致的后代神经发育异常以及ASD样行为。
在胎脑中,巨噬细胞是主要的免疫细胞类型,负责大脑的免疫监视和维持稳态。先前的研究显示,MIA可以增加胎脑中巨噬细胞的活化状态,如CD68表达增加、细胞形态发生改变,从而导致炎症介质如细胞因子和趋化因子的释放。本研究发现MIA可引起胚胎脑膜(meningeal)、脉络丛(choroid plexus)以及胼胝体下纤维束(subcallosal sling)等区域巨噬细胞CD68表达显著增加,表现出明显的激活状态。值得注意的是,抗体清除母体NK细胞可有效缓解这些区域巨噬细胞的激活。因此,母体NK细胞在MIA触发的胎儿脑巨噬细胞的激活中起到了至关重要的作用。
为了探究母体NK细胞通过何种方式介导了胎儿大脑的发育异常,研究团队分选出小鼠蜕膜NK细胞并进行转录组测序,通过差异基因分析筛选出GzmB可能作为关键的致病因子。进一步通过体内实验证明,母体GzmB可以穿过母胎屏障到达胎脑,导致胎脑神经发育异常及成年后的自闭症样行为。采用抑制胞外GzmB活性的抑制剂或者特异性敲除母体NK细胞Gzmb基因均可显著缓解MIA导致的后代神经发育异常。通过单细胞转录组分析进一步发现,蜕膜NK细胞异常释放的胞外GzmB可引起胎脑ISGshigh巨噬细胞增加以及小胶质细胞激活,特异性敲除母体NK细胞来源的GzmB可显著改善胎脑巨噬细胞群体的免疫激活状态。
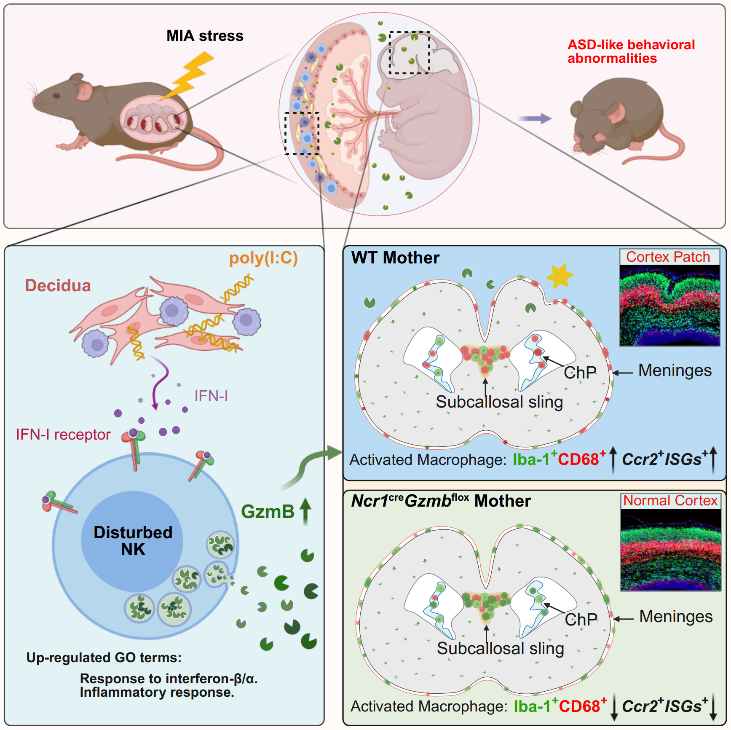
图注:上,孕期病毒感染导致的母体免疫应激影响蜕膜免疫细胞,进而将母体的炎症压力波及至胎脑发育,导致子代成年后自闭症行为;下左,病毒感染导致母胎界面I型干扰素应答,重塑子宫 NK 细胞的功能状态,导致 NK 细胞大量产生细胞外 GzmB;下右,母体 GzmB 可以穿过母胎屏障,导致胎儿脑膜/胼胝体/脉络丛等处出现激活状态巨噬细胞/小胶质细胞,进而影响胎脑发育与成年后行为
该研究揭示了 MIA 诱导子代神经发育障碍和行为异常的全新机制,通过母体子宫NK 细胞异常释放的胞外GzmB介导了后代神经免疫疾病。这项研究横跨生殖免疫与神经免疫两个重要领域,开拓了孕期预防和治疗子代大脑发育以及自闭症等行为问题的途径,强调需要评估子宫内母体免疫细胞作为子代神经发育障碍的潜在因素和治疗干预的目标,对预防和治疗儿童高发神经发育相关疾病具有重要意义。
中国科学技术大学傅斌清教授和魏海明教授为本文共同通讯作者,博士研究生卞启武为论文第一作者。复旦大学丁琛教授对本研究给予了技术指导。该工作得到了中科院先导B项目,科技部重点研发计划,国家自然科学基金等项目资助。
论文链接:https://www.cell.com/immunity/abstract/S1074-7613(25)00191-8

通讯作者介绍
(按照文章通讯作者顺序)

主要从事生殖免疫学研究,研究成果阐明了妊娠早期母胎界面蜕膜NK细胞的免疫调节及促进胚胎发育的重要作用,开发了子宫内膜无创免疫监测系统,并创建了蜕膜样NK细胞转输治疗不明原因反复流产/不孕症的新技术并实现该技术的临床转化。研究成果发表在Immunity, Nature immunology, Science translational Med, PNAS等国际高水平期刊。
教育及工作经历:
2005年毕业于南京大学生物科学系;
2011年于中国科学技术大学微尺度国家实验室获得博士学位;
2011年至2013年间在中国科学技术大学免疫学研究所从事博士后研究;
2013年至2019年间担任中国科学技术大学副研究员/副教授;
2019年担任中国科学技术大学特任教授。
研究方向与兴趣:
1. 母胎界面免疫细胞在妊娠及妊娠相关疾病中的作用;
2. 调控母胎界面免疫细胞发育及功能转化的关键机理;
3. 母体免疫细胞与子代出生缺陷,尤其是神经系统发育障碍的关系;
与此同时,我们还致力于由此衍生出新的针对免疫微环境的临床诊断和治疗方法。
联系方式:
合肥市黄山路443号中国科学技术大学生命学院免疫所
E-mail: fbq@ustc.edu.cn
官网链接获取更多信息:
https://biomed.ustc.edu.cn/2020/0318/c31898a570342/page.htm

联系方式:
E-mail:ustcwhm@ustc.edu.cn
官网链接获取更多信息:
https://biomed.ustc.edu.cn/2023/0530/c31898a604020/page.htm
